Introducción
Desde la descripción clínica inicial de la artritis reumatoide (AR), el pannus ha jugado un papel clave en el desarrollo de la enfermedad y su comprensión ha mejorado junto con el desarrollo de las técnicas histológicas, de biología molecular y de imagen.
En la clínica, el pannus se ha considerado una manifestación tardía, inactiva e irreversible de la enfermedad, aunque el término es puramente histológico. La confusión se hace cada vez más evidente al abordar el seguimiento clínico de la AR y el uso de términos como pannus, sinovitis o sinovitis crónica, con una idea difusa sobre la actividad de la enfermedad.
Para esta revisión se realizó una búsqueda de la literatura en Pubmed y Embase, utilizando los términos pannus, rheumatoid arthritis, ultrasonography, magnetic resonance, desde 1900 hasta 2015. Se buscaron textos y libros no indexados sobre el tema, con el fin de hacer una descripción narrativa e histórica sobre el pannus, su desarrollo y su papel patológico en la AR.
La descripción clínica e histológica inicial del pannus en la artritis reumatoide
Aunque antes de 1859 se habían utilizado términos similares a los de AR, fue Garrod (Fig. 1) quien en el capítulo XV de su libro «The nature and treatment of gout and rheumaticgout «1,2 describió con precisión la enfermedad tal como la conocemos hoy, diferenciándola de la gota y la fiebre reumática. Ofreció ilustraciones detalladas (Fig. 2) de las deformidades típicas y subrayó la gravedad de la enfermedad en comparación con otras afecciones, debido a la dificultad de control de la enfermedad y a su evolución clínica incapacitante (Fig. 3).

Fotografía de Sir. Alfred Baring Garrod, 1819-1907.3
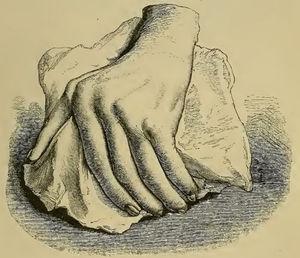
Ilustración del libro de Garrod que representa una mano deformada con desviación cubital resultante de la artritis reumatoide.1,2
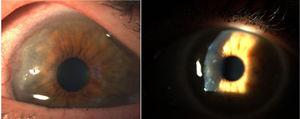
Paneo corneal.8
En 1905 y 1909, Nichols y Richardson en sus trabajos publicados en el Journal of Medical Research y en el Boston Medical and Surgical Journal5 respectivamente, presentaron una de las mejores descripciones clínico-patológicas de las enfermedades reumáticas, y diferenciaron 2 grupos de pacientes: uno que presentaba las características clínicas similares a la AR y otro las características de la artrosis.6 A pesar de que ambos artículos de Nichols y Richardson se refieren a casos de artritis deformante no escrofulosa, la minuciosa representación de las manifestaciones clínicas, acompañada de fotografías e imágenes radiográficas, muestra claramente los casos de AR. Estos autores también recopilaron una serie de muestras histológicas de 75 casos clínicos, llegando a una importante conclusión: existen 2 patrones histológicos de afectación articular, uno de deterioro del cartílago articular y otro de engrosamiento de la membrana sinovial. Este último está estrechamente asociado a la invasión del tejido óseo y del cartílago articular, causando destrucción y ocasionalmente neoformación ósea desorganizada. Esta misma publicación de Nichols y Richardson incluye una descripción de la artritis proliferativa con formación de tejido de granulación muy vascularizado, con un componente celular de origen mesenquimal, principalmente de la membrana sinovial y del llamado tejido tipo pannus. Es la primera vez que se utiliza el término pannus articular.5 Hay que destacar que el término pannus ya se utilizaba en aquella época en oftalmología para describir algún tipo de lesión corneal, y fue definido por la Academia Americana de Oftalmología como un crecimiento de tejido fibroso y vascular entre el epitelio y la membrana de Bowman, presente a menudo en casos de edema corneal crónico, tras la inflamación de la córnea7 (Fig. 7). En ambos casos, pannus sinovial y pannus corneal, las lesiones descritas son similares a un pannus, palabra latina que significa «tela».
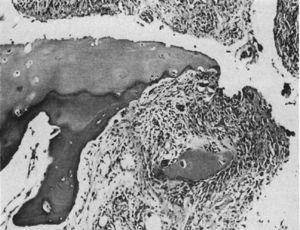
Histología por microscopía óptica. Lesión destructiva en el margen de la articulación interfalángica. Se aprecia el tejido sinovial o pannus junto al tejido de granulación -el llamado movimiento de cierre- que aísla un fragmento del cartílago marcado como «C».9
Algunas de las imágenes y descripciones del estudio de Nichols y Richardson de 19095 se representan en las Figs. 4-6.
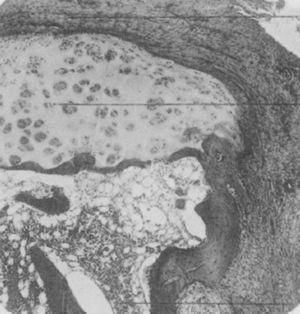
Fotografía de microscopía óptica de la falange distal de un paciente que padece la enfermedad entonces denominada artritis proliferativa de tipo extremo. Muestra la formación de tejido de granulación grueso que invade y destruye el cartílago articular.5,6
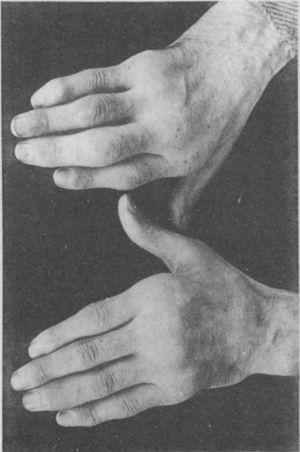
Fotografía de las manos de un paciente de 35 años con antecedentes de uretritis gonocócica, que años después desarrolló progresivamente poliartritis de las articulaciones pequeñas y grandes. Clasificada como artritis proliferativa.5,6
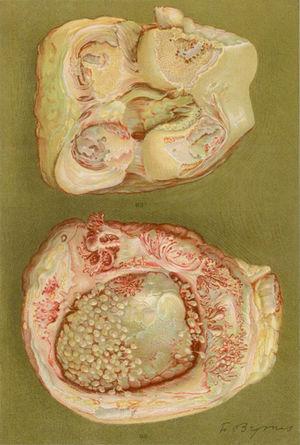
Dibujo de la necropsia de una mujer de 40 años con una clínica de poliartritis de las articulaciones grandes y pequeñas que conlleva una importante discapacidad y anquilosis. Se evidencia pérdida del cartílago articular y zonas de formación ósea dando lugar a anquilosis de rodilla.5,6
En 1959 Kulka publicó una revisión de la patogénesis de la AR,9 tomando como referencia el trabajo de Nichols y Richardson5 , que clasificaba las lesiones histológicas de la AR en 3 tipos: El primer tipo se clasificó como cambios inflamatorios de la membrana sinovial, el segundo como degeneración y necrosis del tejido conectivo, y el tercero como infiltración inflamatoria vascular de las arteriolas y vénulas. El primer tipo de lesiones corresponde al pannus descrito en 1909 por Nichols y Richardson, que consiste en un engrosamiento sinovial que provoca la reabsorción del cartílago. Kulka comprobó mediante microscopía óptica que, por un lado, la lesión destructiva del cartílago se caracterizaba por el crecimiento del tejido sinovial crónicamente inflamado -o pannus- y, por otro, que el tejido de granulación que proliferaba desde los espacios de la médula ósea subcondral y se extendía a través de la placa subcondral para adherirse al pannus y lo rodeaba con un movimiento de pinza, podía progresar hasta aislar fragmentos del cartílago marginal (Fig. 7).9
Kulka en su trabajo definió los criterios histológicos para diagnosticar la AR, si se cumplían al menos 3 de las 5 características distintivas, en ausencia de cualquier otro diagnóstico probable:
-
Proliferación nerviosa
-
Proliferación de las células sinoviales superficiales, generalmente palizada
-
Infiltración marcada de células inflamatorias (linfocitos o células plasmáticas) con tendencia a desarrollar nódulos linfoides
-
Depósito compacto de fibrina
Aunque se hizo hincapié en que ninguna de ellas era específica, la combinación de 3 o más características en ausencia de otras patologías tenía un valor diagnóstico considerable para la AR (Fig. 8).

Histología por microscopía óptica. Sinovitis clásica de rodilla en AR que muestra hipertrofia vellositaria, infiltración vascular y nódulos linfoides con un centro germinal en la esquina derecha.9
Estos investigadores analizaron muestras de la interfase sinovial-cartilaginosa en 8 pacientes con diagnóstico de AR, e identificaron 3 tipos de lesiones: la primera con una infiltración de células mononucleares en los vasos que invaden el cartílago, formando ocasionalmente nidos o agregados celulares dentro de la matriz cartilaginosa (además de células plasmáticas, linfocitos y granulocitos). Además, en el interior de estos nidos también se encontró colágeno circulante disuelto, lo que llevó a la teoría de una secreción enzimática proteolítica (Fig. 9). El segundo tipo de lesiones corresponde a una invasión directa del cartílago de células monocíticas y fibroblastos poco diferenciados que pueden manifestarse como fagocíticas o fibroblásticas, con un contenido citoplasmático granular amorfo con prolongaciones celulares que degradan la matriz colágena cartilaginosa y que pueden verse en el interior de las extensiones celulares (Fig. 10). El tercer tipo de lesión se presenta como una gruesa capa de tejido fibroso y vascularizado que cubre el cartílago e interfiere en la vascularización normal del cartílago articular.

Imagen de microscopio electrónico que muestra fibroblastos con lisosomas inmersos (Lys) y múltiples extensiones citoplasmáticas que invaden la matriz del cartílago (Ctm).10
Durante las siguientes 2 décadas, el papel protagonista del pannus en la fisiopatología de la enfermedad articular en la AR no se limitó a describir la destrucción del cartílago. Edward Harris publicó en 199013 una de las revisiones más completas sobre la fisiopatología de la AR, clasificándola en 5 tipos, de acuerdo con las características inmunológicas del daño articular. Describió que en los estadios iniciales (estadio 2) la sinovia no engrosada y la neovascularización de los macrófagos mediada por citoquinas14 con acumulación de los linfocitos perivasculares desempeñaban un papel importante.15 Como demostró previamente Kobayashi10 mediante microscopía electrónica, los linfocitos -en su mayoría T CD4+16 con escasos reguladores T17 – activan los linfocitos B locales que maduran a células plasmáticas productoras de anticuerpos en el tejido sinovial,18 comprometiendo este tejido como parte del inicio y la progresión de la enfermedad. Harris también afirmó que en estadios más avanzados de la enfermedad (estadio 4) se producía una profusa proliferación de la sinovia con hasta 100 veces su peso normal, lo que se interpretó como un comportamiento similar al de un tumor con aumento de la actividad celular de los sinoviocitos, como se confirmó en medio de cultivo enriquecido donde las células crecían aisladas y de forma autónoma,19 lo que llevó a considerar por primera vez el modelo de los oncogenes, como ocurre en el cáncer.
Componentes celulares del pannus
Aunque varios investigadores continuaron estudiando el componente de tejido engrosado o pannus, no se llegó a un acuerdo con respecto a su patogénesis. En 1983, Burmester et al.20 estudiaron las células no linfocíticas del pannus mediante anticuerpos monoclonales dirigidos contra antígenos de macrófagos y fibroblastos. Identificaron 3 tipos de células de la línea sinovial; las primeras eran en su mayoría (40% del total) células monocíticas o macrófagos con capacidad fagocítica, con receptores Fc y expresión de HLA DR o tipo II. El segundo tipo celular era similar a los monocitos, pero no fagocítico, con expresión de HLA-DR y sin encontrar otros antígenos monocíticos. La última línea celular encontrada era positiva para los marcadores de fibroblastos, pero sin expresión de HLA-DR ni otros antígenos monocíticos (entre el 20% y el 40% del total), lo que se confirmó en 1987 con células clonadas y cultivos celulares.21 La importancia de estas células sinoviales radicaba, entre otros factores, en la activación del protooncogén c-jun en respuesta al estímulo de la IL-a,22 que es similar a las células neoplásicas que aumentan la expresión de colagenasa con capacidad de destruir, junto con la estromelisina y otras metaloproteinasas, la matriz cartilaginosa y ósea,23,24 un hallazgo atribuido previamente a Ziff allá por 1960.11
Zvaifler y Firestein25 en 1994 consideraron que el origen del pannus no estaba claro y que las pruebas se dividían en un tejido sinovial crónicamente inflamado, y un tejido conectivo especializado y altamente vascularizado que se iniciaba en la interfase sinovia-hueso y que históricamente se había definido como el lugar de inicio del proceso destructivo.5,10,26,28 En esta revisión se consideraron dos posibilidades sobre el origen de estos sinoviocitos, que son similares a los fibroblastos y a los que se les dio el nombre de pancitos.20 La primera hipótesis fue que las células mesenquimales inmaduras fueron las primeras en invadir los vasos que penetran en el cartílago y que podrían ser reemplazadas o podrían evolucionar a fibroblastos,27 en un proceso mediado por factores inflamatorios desconocidos (factor X), independientes de los factores derivados de las células T inmunes, como se ha demostrado también en modelos animales.29,30 La segunda hipótesis menos apoyada, y basada en estudios realizados a principios de los años 90,31-33 dependía de las citocinas de los linfocitos y describía la reducción de la expresión del genoma de los linfocitos y de los productos linfocíticos en los tejidos y en el líquido sinovial (Fig. 11).

Vías alternativas a través de las cuales el desconocido factor «X» en la AR podría inducir la formación del pannus. Puede comenzar a través de la vía dependiente de las células T o a través de la vía de los sinoviocitos.25
La revisión de Zvaifler y Firestein25 intenta comprender, no sólo el origen, sino la perpetuación del pannus, basándose en 2 posibilidades: una -como ya se mencionó en 1989- considera un modelo tumoral en el que las células sinoviales son transformadas por una señal que desencadena la proliferación e induce la expresión de oncogenes y la producción de enzimas que degradan la matriz o las proteínas de adhesión.34,35 Estas señales pueden provenir de moléculas solubles como las citoquinas o de agentes etiológicos no especificados. Desde esta perspectiva, tejidos como el cartílago o el hueso, no forman parte de su desarrollo, sino que se ven afectados por el pannus. La segunda posibilidad se basa en la idea de que los compuestos generados por los condrocitos o los complejos inmunes inmersos en el cartílago son los responsables de activar a los sinoviocitos para que invadan el tejido y abandonen su entorno natural.
Sin embargo, no se ha establecido el proceso por el que los sinoviocitos similares a los fibroblastos, que carecen de receptores Fc, se ven afectados por estos complejos inmunes36, pero es probable que las células monocíticas-macrófagas sean las intermediarias. Una explicación probable de este suceso es la unión de las proteínas del complemento y los complejos inmunes a la vitronectina y sus receptores, que afecta a la diferenciación, migración y proliferación de los fibroblastos y que posteriormente se amplifica por el contacto de estas células con el colágeno, la fibronectina y otras metaloproteinasas,37,38 a través de la expresión de receptores como VCAM-1, que hasta entonces era la única molécula de adhesión conocida sobreexpresada en los sinoviocitos similares a los fibroblastos.39
Según este segundo escenario, el cartílago no sólo sería el tejido afectado por el pannus, sino el inductor y perpetuador de esta respuesta. No obstante lo anterior, sigue estando claro que la conservación del pannus depende de las citoquinas que estimulan el crecimiento celular y de la producción de enzimas sintetizadas por los sinoviocitos derivados de monocitos40 y de los sinoviocitos similares a los fibroblastos. Se demostró in vitro que las enzimas se sintetizaban41 a través de la regulación e intermediación de los linfocitos T, los monocitos y sus subproductos, que representan la mayor parte de las células del pannus.42
El trabajo de Burmester en 198320 fue fundamental para la continuidad del estudio del componente celular del pannus. El grupo de Xue en 1997 estudió especímenes de artroplastia que contenían pannus de pacientes con AR y observó células del PSC que fueron estudiadas fenotípicamente mediante microscopía e inmunohistoquímica, con una expresión proteica y genómica específica.43 Estas células resultaron ser positivas para los filamentos de vimentina, marcadores de inmunofluorescencia (Fig. 12) y eran morfológicamente similares a los fibroblastos bajo el microscopio. Sin embargo, el marcador safranina O que reacciona con los proteoglicanos (Fig. 13), así como la expresión de ARNm del colágeno tipo II que se utiliza para identificar las células similares a los condrocitos, también fueron positivos; de ahí la conclusión de que estas células son una combinación de fibroblastos y condrocitos.
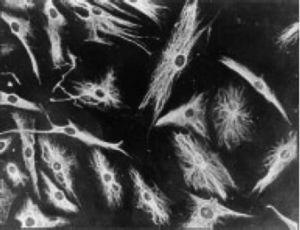
Micrografía de inmunofluorescencia que muestra la positividad de las células del PSC a los anticuerpos anti-vimentina marcados con isotiocianato de fluoresceína. Esto es similar a los hallazgos en los fibroblastos.43
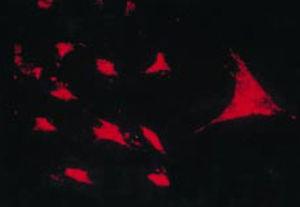
Ensayo de transcriptasa inversa in situ para mostrar la expresión de ARN de colágeno tipo II en un cultivo de PSC, que transmite características similares a las de los condrocitos.43
El estudio de expresión del genoma también evidenció la alta actividad de los proto-oncogenes para c-myc, c-jun y c-fos que permite la alta producción de enzimas como la catepsina B y L y algunas colagenasas.
En años posteriores se revelaron más pruebas sobre las características del tejido en la enfermedad articular temprana y el aumento de la expresión del gen p53,44 mutaciones que se observaban con más frecuencia en los estadios avanzados.45 En 2003, Smeets et al. observaron diferencias en las características celulares, la expresión de citocinas, los factores angiogénicos y las metaloproteinasas del pannus, obtenidas a partir de muestras de pacientes con enfermedad tardía que se sometían a una sustitución articular sin signos de actividad clínica de la artritis, en comparación con los pacientes que se sometían a una artroscopia y que se consideraban en las primeras fases de la enfermedad porque todavía tenían actividad clínica de la artritis.46 Las diferencias entre ambos grupos fueron el mayor número de macrófagos y linfocitos T derivados de las muestras de artroscopia o de enfermedad temprana, y la mayor expresión de TNF-a, IL-6, metaloproteinasas (MMP-1, MMP-3, MMP-13) y del factor de angiogénesis (VEGF).
El pannus suele considerarse un tejido fibroso sin mayor actividad biológica y un remanente del daño articular que parece ser irreversible. Sin embargo, el pannus se comporta como un medio productor de grandes cantidades de enzimas proteolíticas, con un papel patológico central, como las MMP 1, 3, 13 y 14.47 La MMP 3 o estromelina (mencionada anteriormente)23,24,48 en particular, se produce intensamente como se demostró en 200549 mediante la detección de ARNm en la unión sinovial-cartilaginosa, y es dependiente de la IL-1b para la estimulación de la síntesis. La MMP 3 se diferencia de la MMP 1 o colagenasa tipo 1, porque es menos abundante y es estimulada por el TNF-a.
Pannus y el factor nuclear kappa B
El factor de transcripción nuclear kappa B (NF-kB) es uno de los reguladores más importantes de la transcripción genómica de citoquinas, quimioquinas y moléculas de adhesión; Desempeña un papel en la degradación del cartílago y del hueso articular,50 y está aumentado tanto en el tejido sinovial de los pacientes como en los modelos animales con AR,51-53 principalmente en la unión entre el pannus y el cartílago53 , donde hay un mayor número de células productoras del factor, en comparación con otros lugares sinoviales fuera de esta unión. La relevancia del factor NFkB en cuanto al daño articular no sólo se refleja en el aumento del número de citocinas, sino en la osteoclastogénesis, un proceso clave en la erosión ósea,54,55 que depende de la línea mieloide y del complejo RANK-RANKL,56-58 permitiendo la activación, migración y supervivencia del osteoclasto.59,60 El RANKL procede de los linfocitos T, de los sinoviocitos similares a los fibroblastos y de las células que se encuentran fuera de la interfase entre el pannus y el hueso.50,61-63 Pettit et al., en 2006,64 estudiaron el patrón de expresión del RANKL, el NF-kB y la osteoprotegerina (inhibidor natural del RANKL que bloquea su unión al receptor y, por tanto, impide la osteogénesis) en muestras de pannus de pacientes con AR, concretamente de la interfase entre el pannus y el hueso, donde nunca se había estudiado. El resultado fue que tanto el RANKL como la osteoprotegerina se expresan en los microambientes donde el pannus interactúa con el hueso o el cartílago y hay erosión o daño tisular, siempre en proporciones que favorecen la maduración del osteoclasto y su activación. Este desequilibrio molecular fue ratificado en 2008.65
Imágenes de diagnóstico y pannus
En 1978 Cooperberg fue el primero en mostrar la sinovitis con ultrasonidos, observando un engrosamiento de la membrana sinovial de la rodilla en una imagen en escala de grises.66 Se observaron más detalles en el trabajo de De Flaviis en 1988, implementando un protocolo de ultrasonidos en la mano de pacientes con AR.67 Pasaron 6 años hasta que Newman utilizó el método Doppler en tendones y bursas,68 y 2 años después lo utilizó para el engrosamiento sinovial en las rodillas de pacientes con AR.69 Natias Hau, en 1999, con ultrasonidos de alta resolución, utilizó por primera vez el modo Doppler en el pannus de las manos de pacientes con AR, mostrando la hipervascularización70 de las articulaciones de la rodilla, confirmando así la mayor vascularización ya descrita en estudios realizados un siglo antes (Fig. 14).5,12,14,15
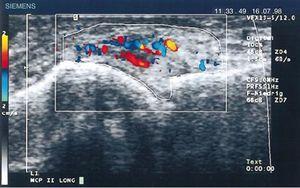
Una ecografía longitudinal de la articulación metacarpofalángica que muestra las primeras imágenes Doppler con aumento de la vascularización del pannus en un paciente con AR.70
El uso de la resonancia magnética que se inició en 1988 con el trabajo de Gilkenson demostró que era un mejor método para detectar las erosiones de la mano en pacientes con AR79; Kusunoglu en 1990 demostró que era útil para diferenciar el engrosamiento sinovial del derrame articular.80 La visualización del pannus mediante este método comenzó en 1994, cuando por primera vez Ostergaard evaluó el crecimiento sinovial y su relación con la actividad de la enfermedad,81 confirmado por un trabajo más extenso de Sugimoto en 1998,82 y finalmente en 2003 el grupo OMERACT definió la sinovitis en la resonancia magnética nuclear como un aumento del grosor sinovial tras la inyección de contraste; esto es definitivamente la evidencia de pannus.83
Conclusiones
La historia ha permitido comprender el papel crítico del pannus en la destrucción articular, que en ocasiones es similar a una lesión tumoral por su rápido y abundante crecimiento, favoreciendo la producción de anticuerpos que perpetúan el proceso autoinmune. Esto contraviene la idea de que el pannus es un tejido de granulación apenas activo, que se limita a ser un mero tejido cicatricial residual. Estas características interfieren con los procesos de desarrollo, progresión y destrucción del hueso y el cartílago articulares que se han evidenciado durante más de 100 años, y se han comprobado con técnicas de microscopía y biología molecular. Por lo tanto, la idea de que el pannus es una condición definitiva o irreversible es incorrecta, ya que no es una parte activa de la enfermedad y, por el contrario, puede revertirse en respuesta al tratamiento. El uso incorrecto del término debe evitarse para que la evaluación clínica de la enfermedad sea menos confusa. Estos cambios se han atribuido históricamente a la sinovitis, que es simplemente la inflamación del tejido sinovial evaluada clínicamente. El término sinovitis no se puede diferenciar del pannus, ya que se refiere a un hallazgo histológico y, por tanto, el pannus no está comprendido en la evaluación clínica inicial ni en el seguimiento de los pacientes con AR por parte de las distintas sociedades científicas.
Por lo tanto, nuevos estudios sobre el pannus como componente indispensable de la patogénesis de la AR contribuirán a una mejor comprensión de la enfermedad desde su mismo inicio, y abrirán nuevas vías para su evaluación clínica o de imagen, además de identificar terapias más específicas que inhiban la destrucción de las articulaciones.
Conflicto de intereses
Los autores no tienen ningún conflicto de intereses que revelar.