Corrosie is een natuurlijk destructief verschijnsel dat optreedt wanneer sommige metalen aan het milieu worden blootgesteld. De reactie tussen lucht, vocht en het metalen substraat leidt tot specifieke chemische reacties die ertoe leiden dat het metaal wordt omgezet in zijn chemisch meer stabiele oxide-, hydroxide- of sulfidevorm. Bij ijzerhoudende metalen, zoals staal, treedt corrosie op in de vorm van ijzer-III-oxiden, ook wel roest genoemd.
Om elektrochemische corrosie te laten optreden, moeten drie ingrediënten aanwezig zijn: een anode, een kathode en een elektrolyt. De anode en de kathode zijn gewoonlijk via een ononderbroken elektrisch pad met elkaar verbonden, terwijl beide in dezelfde elektrolyt zijn ondergedompeld. Tijdens dit proces treedt corrosie op bij de anode, terwijl de kathode onaangetast blijft.

Figuur 1. Een typische elektrochemische cel met elektronen die van de anode naar de kathode stromen via een elektrische verbinding. (Bron: Alksub op de Engelse Wikipedia / CC BY-SA)
Er zijn verschillende methoden om corrosie te voorkomen en te beheersen. Een daarvan staat bekend als kathodische bescherming (CP). Deze techniek werkt door het te beschermen metaal te verbinden met een gemakkelijker te corroderen “opofferingsmetaal”. Dit opofferingsmetaal corrodeert bij voorkeur (het fungeert als anode) terwijl het waardevoller metaalobject in kwestie (het fungeert als kathode) beschermd blijft. In dit artikel wordt uitgelegd hoe deze opofferingsmethode werkt en worden de verschillende toepassingen beschreven.
Galvanische of bimetallische corrosie
Om te begrijpen hoe kathodische bescherming werkt, moeten we eerst de basisprincipes van bimetallische corrosie begrijpen, ook bekend als galvanische corrosie. Bimetaalcorrosie is, zoals de naam al aangeeft, een uniek type corrosie dat optreedt tussen de koppeling van twee metalen. Deze corrosie wordt waargenomen in verschillende situaties waarin ongelijke metalen direct of indirect met elkaar in contact komen. Bimetaalcorrosie wordt gewoonlijk gekenmerkt door versnelde corrosie in één metaal, terwijl het andere metaal onaangetast blijft. Met andere woorden, het ene metaal offert zich op terwijl het het andere beschermt. (Dit proces wordt uitvoeriger onderzocht in het artikel Waarom veroorzaken twee ongelijke metalen corrosie?)
Corrosie in een elektrochemische cel wordt hoofdzakelijk aangedreven door een eigenschap die bekend staat als potentiaalverschil. Dit potentiaalverschil zorgt ervoor dat elektronen van het ene metaal in de cel (de anode) naar het andere metaal (de kathode) stromen, terwijl daarbij een kleine hoeveelheid elektriciteit wordt opgewekt. Naarmate elektronen uit de anode stromen, treedt oxidatie op, waardoor het anodische metaal wordt afgebroken of corrodeert. Ondertussen, als elektronen naar de kathode stromen, vindt reductie plaats, waardoor het kathodische metaal verder wordt beschermd.
Bij bimetallische corrosie is dit potentiaalverschil een direct resultaat van het verschil in elektrodepotentiaal tussen de twee ongelijke metalen. Wanneer een metaal in een elektrolyt wordt ondergedompeld, neemt het een elektrodepotentiaal aan dat de capaciteit van het metaal vertegenwoordigt om worden geoxydeerd of worden verminderd. De elektrodepotentiaal van verschillende metalen wordt weergegeven op een lijst die bekend staat als de galvanische reeks. (Zie Een inleiding tot de Galvanische reeks: Galvanische compatibiliteit en corrosie voor meer informatie). De metalen die hoger op de tabel staan worden beschouwd als anodisch (meer elektronegatief), terwijl de metalen die lager op de tabel staan meer kathodisch (meer elektropositief) zijn. Hoe verder de contacterende metalen in de galvanische reeks uit elkaar liggen, hoe groter het potentiaalverschil tussen de metalen, en dus hoe ernstiger de corrosie aan de anode.
Kathodische bescherming (CP) en haar werkwijze
Hoewel het ontwerp van kathodische beschermingssystemen ingewikkeld kan zijn, is hun werking gebaseerd op het concept van bimetallische of galvanische corrosie dat eerder werd beschreven. Door de principes van dit type corrosie te begrijpen, kunnen wij doelbewust metalen aan elkaar koppelen om ervoor te zorgen dat het ene kathodisch het andere beschermt. Met andere woorden, als wij een bepaalde metaalstructuur willen beschermen, kunnen wij omstandigheden creëren waarin dit metaal de kathode wordt van een elektrochemische cel. Door het te beschermen metaal elektrisch te verbinden met een meer anodisch (elektronegatief) metaal, kunnen we ervoor zorgen dat de anode zich opoffert door bij voorkeur te corroderen boven zijn kathodische tegenhanger.
In sommige gevallen kunnen externe stroombronnen worden gebruikt om extra elektronen aan het elektrochemische proces te leveren, wat de effectiviteit van kathodische bescherming kan verhogen.
Kathodische beschermingssystemen worden in tal van industrieën gebruikt om een breed scala van structuren in uitdagende of agressieve omgevingen te beschermen. Met name de olie- en gasindustrie maakt gebruik van kathodische beschermingssystemen om corrosie in brandstofpijpleidingen, stalen opslagtanks, offshore platforms en oliebronomhulsels te voorkomen. In de maritieme industrie wordt deze beschermingsmethode ook gebruikt op stalen palen, pieren, steigers en scheepsrompen. Een ander veel voorkomend type kathodische bescherming, bekend als galvaniseren, wordt gewoonlijk gebruikt om stalen onderdelen en constructies te beschermen. (Voor meer informatie, lees Galvaniseren en zijn Efficiëntie in Corrosiepreventie.)
Types van Kathodische Bescherming (CP)
Zoals eerder vermeld, werkt kathodische bescherming door opzettelijk een galvanische cel te vormen met een ander opofferingsmetaal. Dit kan worden bereikt door twee verschillende soorten kathodische bescherming te gebruiken: passieve kathodische bescherming en geïmponeerde stroom kathodische bescherming.
Passieve kathodische bescherming
In passieve kathodische beschermingssystemen is de opofferingsanode direct of indirect verbonden met het te beschermen metaal. Het potentiaalverschil tussen de twee ongelijke metalen wekt voldoende elektriciteit op om een elektrochemische cel te vormen en galvanische of bimetallische corrosie te veroorzaken.
Dit type bescherming wordt vaak gebruikt in de olie- en gasindustrie om de stalen constructiedelen van offshore booreilanden en platforms te beschermen. Hier worden aluminiumstaven (of een ander geschikt metaal) rechtstreeks op stalen secties gemonteerd om de rol van het opofferingsmetaal op zich te nemen. Stalen boilers, tanks en palen worden ook volgens een soortgelijke methode kathodisch beschermd.
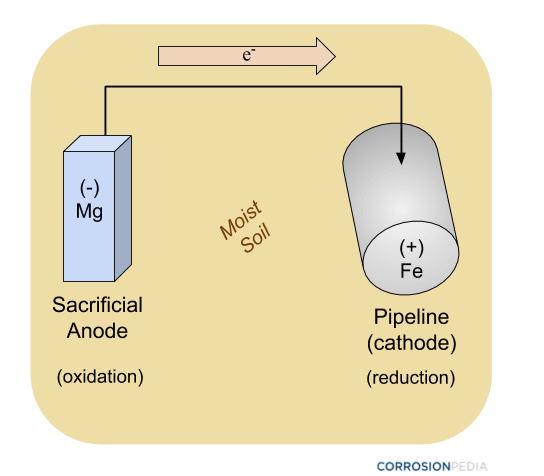
Figuur 2. Schema van een pijpleiding die wordt beschermd door een opofferingsanode met behulp van passieve kathodische beschermingsmethoden.
Een ander veel voorkomend voorbeeld van passieve kathodische bescherming is thermisch gegalvaniseerd staal. Tijdens dit proces worden stalen onderdelen of constructies ondergedompeld in een bad van gesmolten zink dat het object bedekt. Wanneer het staal uit het gesmolten zink wordt verwijderd, reageert het met lucht en vocht om een beschermende laag te vormen die zinkcarbonaat wordt genoemd en die een galvanische cel met het staal vormt.
Wanneer het stalen lid wordt gekrast of beschadigd, zodat het substraat bloot komt te liggen, fungeert de omringende zinklaag als de opofferingsanode en corrodeert bij voorkeur om het blootgestelde staal te beschermen. Dit type bescherming gaat door totdat het zink in de omgeving is uitgeput.
Impressed current cathodic protection (ICCP)
In grote constructies kan het niet haalbaar zijn om passieve kathodische beschermingsmethoden te gebruiken. Het aantal opofferingsanoden dat nodig is om voldoende stroom te leveren voor een adequate bescherming kan onrealistisch of onpraktisch zijn. Om dit te verhelpen wordt een externe stroombron gebruikt om de elektrochemische reacties aan te drijven. Deze techniek staat bekend als “impressed current cathodic protection” (ICCP). ICCP-systemen zijn ideaal voor de bescherming van lange structuren, zoals ondergrondse pijpleidingen. De flenzen van verbindingspijpen worden gewoonlijk geïsoleerd met behulp van isolatiesets om de pijpen in kleinere, beter hanteerbare secties te scheiden met het oog op ICCP-bescherming.

Figuur 3. Schema van een object dat wordt beschermd door een anode met behulp van geïmponeerde stroomkathodische bescherming (ICCP).
Beperkingen van kathodische bescherming
In grote pijpleidingnetwerken kunnen er veel kruisingen, parallellen en naderingen zijn in de buurt van het CP-systeem van de pijpleiding. Tussen pijpleidingen kunnen gelijkstroomstoringen optreden, wat corrosie versnelt. Om dit probleem te ondervangen, kunnen pijpleidingen elektrisch worden gekoppeld, hetzij direct, hetzij via weerstand.
Bij gecoate pijpleidingen kan kathodische disbondment optreden als gevolg van hoge CP-niveaus waarbij de aangebrachte coatingkwaliteit slecht is. Hogere temperaturen kunnen ook kathodische disbondment bevorderen. Hoge pH-waarden zijn ook een probleem in termen van scheurvorming door spanningscorrosie.
Conclusie
Kathodische bescherming is een populaire beschermingsmethode voor het voorkomen van corrosie in pijpleidingen, offshore olieplatforms en andere stalen constructies. Voor een effectieve toepassing is het echter van cruciaal belang om de basisprincipes van bimetallische/galvanische corrosie te begrijpen. De keuze van het juiste type kathodisch beschermingssysteem hangt af van verschillende factoren, waaronder de kosteneffectiviteit en de omvang van de te beschermen constructie.