Esophageal motility disorders are often a neglected condition. Niet alleen overlappen de niet-specifieke klinische presentaties zoals brandend maagzuur, pijn op de borst en chronische hoest vaak met de andere veel voorkomende aandoeningen, maar er is ook een gebrek aan apparatuur om de slokdarmfunctie te testen.
De slokdarmmotoriek werd vroeger geëvalueerd door middel van conventionele manometrie, waarbij de resultaten in lijntracering werden weergegeven. In 2001 stelden Spechler en Castell1 voor deze gegevens toe te passen om oesofageale manometrische stoornissen in 4 groepen in te delen:
1. Ontoereikende ontspanning van de onderste slokdarmsfincter (LES) die klassieke achalasie of atypische stoornissen van de LES ontspanning kan zijn.
2. Ongecoördineerde slokdarm lichaam contractie verwijzend naar diffuse slokdarm spasme.
3. Slokdarm hypercontractie die kan optreden bij het lichaam (nutcracker esophagus) of LES (hypertensieve LES).
4. Hypocontractie van het slokdarmlichaam wat ineffectieve slokdarmmotiliteit (IEM) betekent.
In 1991 begonnen Clouse et al,2 met het maken van topografische slokdarmplots van een conventionele manometrische studie, en onthulden een grotere diagnostische nauwkeurigheid voor slokdarmdysmotiliteit.3 Tijdens de DDW bijeenkomst van 2007 in San Diego, werkte de werkgroep hoge resolutie manometrie (HRM) voor het eerst samen om de oesofageale druk topografie (EPT) aan te passen om klinische oesofageale dysmotiliteit te beoordelen. In 2008 publiceerden Kahrilas et al.4 de eerste Chicago classificatie (CC) met behulp van oesofageale druktopografie voor het diagnosticeren van slokdarmmotiliteitsstoornissen, en later in 2012 en 2015 werden CC versie 2.0 en 3.0 aangekondigd, respectievelijk.5,6
Volgens CC versie 3.0, wordt oesofageale dysmotiliteit voornamelijk geclassificeerd in;
1. Slecht ontspannende LES die achalasie of esophagogastric
junction (EGJ) outflow obstructie zou kunnen zijn.
2. Grote stoornissen van peristaltiek: afwezige contractiliteit, distale slokdarm
spasme of jackhammer slokdarm en
3. Kleine stoornissen van peristaltiek: IEM of gefragmenteerde peristaltiek.6
Hypotensieve (eind expiratoire rust LES druk < 10 mmHg met normale peristaltiek) en hypertensieve LES (eind expiratoire rust LES > 35 mmHg met normale peristaltiek en EGJ relaxatie) beide genoemd in CC versie 1.04 is niet verder uitgegeven in versie 2.0 en 3.0.5, 6 Elke slokdarmmotiliteitsstoornis zoals vermeld in CC versie 3.0 zal in dit artikel de revue passeren.
Achalasie
Idiopathische achalasie is een primaire slokdarmaandoening die wordt gekenmerkt door verlies van slokdarmperistaltiek en stoornis in de relaxatie van de LES.7 Bij ongeveer 3-4% van de patiënten met verdenking op achalasie is sprake van pseudoachalasie,8 een aandoening die optreedt wanneer kwaadaardige cellen infiltreren en de plexus myentericus van de distale slokdarm of EGJ vernietigen. Idiopathische achalasie is een zeldzame ziekte. De incidentie is 0,3-1,63 per 100.000 volwassenen per jaar,9-13 en de prevalentie is 8,7-11,2 per 100.000 volwassenen in 10 jaar.9,13,14
De pathogenese van achalasie is de gestoorde functie of het verlies van postganglionale remmende neuronen in de plexus myentericus, die de gladde spieren van de distale slokdarm en de EGJ voeden door twee neurotransmitters af te scheiden: vasoactief intestinaal polypeptide (VIP) en stikstofmonoxide (NO).15, 16 Al deze factoren samen leiden tot slokdarmaperistaltiek en een slecht ontspannen LES.17 Cytotoxische lymfocyten- en/of complementactivatie kan deze chronische ganglionitits veroorzaken, vooral bij patiënten met HLA DQA1*0103 en HLA DQB1*0603 allelen.18 Van sommige virussen, bijvoorbeeld herpes simplex virus-1 (HSV-1), mazelen, humaan papillomavirus (HPV) en varicella zoster virus (VZV), wordt verondersteld dat ze betrokken zijn bij de pathogenese van idiopathische achalasie. Geen enkele studie heeft deze associatie echter definitief aangetoond.17, 19 De klinische manifestaties van idiopathische achalasie correleren vermoedelijk met de graad van oesofagale pathologie. In eerste instantie presenteren patiënten met oesofageale myenterische neuritis of ganglionitis zich overwegend met krachtige achalasie (type III achalasie). Vervolgens, wanneer het inflammatoire proces resulteert in een verlies van ganglioncellen en neurale fbrosis, zullen patiënten uiteindelijk klassieke achalasie (type I) of achalasie met compressie (type II) ontwikkelen.17
Meer dan 90% van de patiënten met achalasie presenteert zich met dysfagie van vaste en vloeibare stoffen. Andere symptomen zijn brandend maagzuur, regurgitatie van onverteerd voedsel, niet-cardiale pijn op de borst en gewichtsverlies. Daarnaast kunnen ook respiratoire symptomen, zoals heesheid, keelpijn, hoest en pulmonale aspiratie worden aangetroffen bij patiënten met achalasie.19, 20 Esophagogastroduodenoscopie (EGD) moet worden uitgevoerd bij patiënten met dysfagie om mechanische obstructie uit te sluiten; de sensitiviteit is echter laag voor het diagnosticeren van achalasie, vooral in het vroege stadium.19 De EGD-bevindingen die kunnen worden gevonden bij achalasie zijn een verwijde of kronkelige slokdarm, achtergehouden voedsel in het slokdarmlumen, slokdarm candidiasis en enige weerstand bij het passeren van de gastroscoop door de EGJ.20
Barium-esofagografie heeft ook een lage sensitiviteit voor het vaststellen van het vroege stadium van achalasie. Bij idiopathische achalasie kunnen slokdarmdilatatie en een vogelbek-achtig uiterlijk worden gevonden. Voorzichtigheidshalve, als de lengte van de distale slokdarmvernauwing groter is dan 3,5 cm en de proximale slokdarmdilatatie minder dan 4 cm, moet de arts verdacht zijn op pseudoachalasie.21
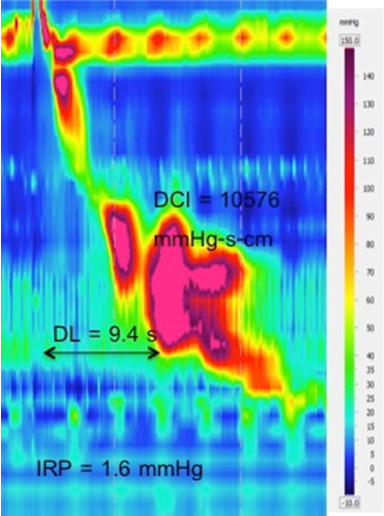
Volgens de huidige CC versie 3.0, wordt achalasie in 3 typen geclassificeerd. De criteria voor de diagnose van type I achalasie is verminderde EGJ relaxatie met 100% mislukte peristaltiek (figuur 7). Gefragmenteerde peristaltiek is aandoening waarbij ten minste 50% gefragmenteerde contractie optreedt (een slik met DCI > 450 mmHg-s-cm en breuk > 5 cm lengte in de 20-mmHg isobare contour) (figuur 7).6 Bij al deze slokdarmhypomotiliteitsstoornissen moet sprake zijn van een normaal ontspannende LES.
Op dit moment is de behandeling van slokdarmhypocontractie voor herstel van de slokdarmperistaltiek nog beperkt. De huidige behandeling is gericht op het aanpakken van concomitante GERD, die vaak wordt aangetroffen bij deze motiliteitsziekte.69 Aanpassing van de levensstijl kan de oesofageale bolustransit verhogen en de blootstelling aan oesofageaal zuur verminderen.69 Het grondig kauwen van voedsel, het consumeren van vloeibaar en halfvast voedsel, het drinken van veel water en het gebruik van koolzuurhoudende dranken kunnen de oesofageale bolustransit bevorderen en bolusretentie voorkomen.69 Gewichtsvermindering, vermijden van onmiddellijke lighouding na de maaltijd, verhoging van het hoofd van het bed, linker laterale decubituspositie en vermijden van vette voedingsmiddelen of calorierijke diëten kunnen helpen bij het verminderen van de blootstelling van de slokdarm aan zuur en/of de frequentie van reflux-symptomen.78, 79 Bovendien zijn er verschillende studies die aantonen dat kauwen op kauwgom de blootstelling van de slokdarm aan zuur kan verminderen en de reflux-symptomen bij patiënten met GERD kan verlichten.80-82
Farmacologische behandeling bij patiënten met oesofageale hypocontractie bestaat uit zuuronderdrukkingstherapie, alginaatvormend intra-gastrisch vlot dat zowel zure als niet-zure refluxen remt, en prokinetica zoals domperidon, metoclopramide, macroliden en serotoninereceptor agonist en/of antagonist.69 Fundoplicatie is een effectieve langetermijnbehandeling voor het voorkomen van gastro-oesofageale reflux. Hoewel patiënten met ernstige oesofageale hypomotiliteit terughoudend moeten zijn voor deze operatie, is deze aandoening geen absolute contra-indicatie.83 Bovendien zijn er aanwijzingen dat fundoplicatie de slokdarmfunctie kan verbeteren bij patiënten met GERD en oesofageale hypomotiliteit.84,85
Concluderend: oesofageale motiliteitsstoornissen, waaronder LES-disfunctie en oesofageale peristaltische afwijking, zijn belangrijke aandoeningen. Ze worden echter vaak ondergediagnosticeerd omdat sommige klinische presentaties overlappen met GERD, die in de dagelijkse praktijk vaker wordt aangetroffen. Bovendien is slokdarmmanometrie niet algemeen beschikbaar en zijn huisartsen mogelijk niet bekend met deze geavanceerde slokdarmfunctietest. Nader onderzoek met slokdarmmanometrie bij patiënten met refractaire slokdarmklachten (zoals brandend maagzuur, regurgitatie en niet-cardiale pijn op de borst) en/of ademhalingsklachten (zoals chronische hoest) met onduidelijke oorzaken zou de unieke slokdarmdysmotiliteitsstoornis aan het licht kunnen brengen. Dit zou artsen kunnen helpen bij het kiezen van de juiste behandeling voor hun patiënten.