O uso de ligantes de fosfato é um dos elementos básicos no tratamento de CKD-MBD (“Chronic Kidney Disease-Mineral and Bone Disorder”).1
É bem conhecido há décadas que a retenção de fosfatos através de mecanismos directos e indirectos, contribui para a geração e progressão do hiperparatiroidismo secundário (SHP) e da osteodistrofia renal na doença renal crónica (CKD).1,2 De facto, a retenção de fosfatos bloqueia todos os mecanismos hormonais contra-regulatórios, aumenta a resistência esquelética ao PTH e é considerada um factor central na fisiopatologia de outras alterações endócrinas e sistémicas como a diminuição do calcitriol, aumento do factor de crescimento fibroblástico-23 (FGF-23), calcificações cardiovasculares, envelhecimento precoce e a elevada morbi-mortalidade destes doentes.2,3 Por tudo isto, o fosfato tem sido considerado como “o assassino silencioso” de pacientes com CKD.4
Como consequência, especialmente em pacientes de diálise, as recentes directrizes do KDIGO sublinham a importância da restrição alimentar com fosfato, uma dose adequada de diálise e o uso de ligantes de fosfato.2 A evidência sobre o efeito positivo da dieta é limitada e de baixa qualidade5 e uma restrição agressiva de fosfatos não só é difícil como também pode comprometer o estado nutricional do paciente, contrabalançando o benefício do controlo do fósforo.6 De facto, o uso de ligantes de fosfato permitiria uma dieta mais liberal e uma diminuição do risco de desnutrição.6Embora, por definição, todos os ligantes de fosfato diminuam os níveis séricos de fosfato, as características dos ligantes de fosfato (com cálcio, sem cálcio, com metais como o magnésio, ferro ou alumínio; polímeros), em monoterapia ou combinação, parecem condicionar os efeitos diferenciais numa variedade de aspectos do complexo CKD-MBD (isto é, calcificação arterial, níveis FGF-23) ou na sobrevivência dos pacientes de diálise.7,8 As novas directrizes KDIGO 2017 aumentaram o grau de evidência sobre a necessidade de restringir o uso de ligantes fosfatados contendo cálcio em todos os doentes com CKD (evidência 2B)2 e esta restrição não se aplica apenas aos doentes com hipercalcemia, calcificação arterial, doença óssea adinâmica ou doentes com paratormona (PTH) persistentemente reduzida, como sugerido nas directrizes anteriores. Do mesmo modo, ainda é considerado razoável avaliar a presença de calcificações vasculares/valvulares em doentes com CKD para orientar a gestão farmacológica.2,9
Aglutinantes: aderência e interacções farmacológicas
Nefrologistas estão geralmente conscientes de que os doentes com CKD, especialmente em terapia de substituição renal, têm de tomar um grande número de fármacos e muitos deles são aglutinantes de fosfato sob a forma de comprimidos/cápsulas/sachês diários.10 A administração simultânea de vários fármacos ao mesmo doente é muito frequente. Embora esta situação possa ser benéfica para melhorar a aderência terapêutica, existem alguns inconvenientes, como a possibilidade de interacções farmacológicas, especialmente em pacientes de idade avançada ou com patologias crónicas.
Um aspecto frequentemente esquecido pelos nefrologistas é que os ligantes de fosfato, devido às suas diferentes propriedades bioquímicas, podem ter uma influência diferencial marcada na absorção e eficácia de muitos medicamentos. De facto, a sua administração simultânea com outros fármacos é frequente e as suas possíveis implicações clínicas podem ser frequentemente despercebidas. Assim, consideramos importante melhorar esta prática e rever as interacções farmacológicas descritas nos diferentes aglutinantes de fósforo.
Interacções farmacológicas
O diferente efeito dos aglutinantes de fosfato na absorção de outros medicamentos implica uma interacção farmacocinética (afectando geralmente a absorção) que é diferente das interacções farmacodinâmicas (afectando a ligação aos receptores ou alterando os mecanismos de transdução de sinal). Existem muitas revisões e tabelas que resumem os diferentes efeitos dos ligantes de fosfato (dose, número de comprimidos, efeitos secundários, níveis de cálcio, fosfato, PTH, FGF-23 e mesmo sobre a progressão da calcificação vascular e/ou sobrevivência/mortalidade)9; contudo, não existem publicações que analisem e comparem possíveis interacções medicamentosas como as resumidas na figura 1. Pode-se observar que a maioria das interacções medicamentosas são observadas com ligantes de cálcio e alumínio contendo fosfato.

aumenta o risco de hipercalcemia e toxicidade farmacológica secundária (i.e. digitalis). Em branco, nem Sevelamer nem lanthanum foram estudados com diuréticos, mas a hipercalcemia não é um efeito secundário.

sem interacção (demonstrado em estudos in vitro ou in vivo).

interacção não especificada.

Não descrito mas com um potencial efeito de classe.

Demonstrou a ausência de interacção também com furosemida e losartan.>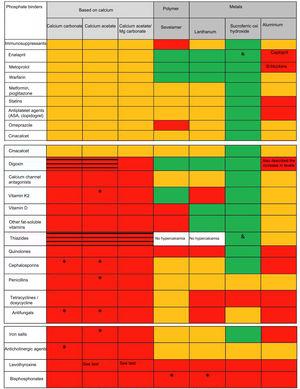
Interacções farmacológicas de grande significado nefrológico dos diferentes ligantes de fosfato disponíveis em Espanha.
# Ver texto. O hidróxido de alumínio pode aumentar a concentração de ácido valpróico (embora o seu significado clínico não esteja estabelecido) e foram descritas intoxicações para a quinidina e a digoxina. Para além das apresentadas, reduz a absorção ou diminui os níveis de alopurinol e sucralfate, AINEs, carbenoxolona, clorpromazina, epoetina, cetoconazol, etambutol, gabapentina, isoniazida, metronidazol, penicilamina, ranitidina, cloroquina, ciclinas, diflunisal, fluoreto de sódio, glucocorticóides, caiaxalato, lincosamidas, fenotiazinas e neurolépticos, cefpodoxima, isoniazida e nitrofurantoína. Deve ser mencionada a diminuição da absorção de corticosteróides, embora com repercussões clínicas duvidosas se a resposta ao fármaco for monitorizada. Sabe-se que a toxicidade é aumentada pelo citrato de sódio e vitamina C. Aumenta a excreção do ácido acetilsalicílico e pode alterar a distribuição do pertecetato de sódio em testes de radioimagem.

Resorção reduzida/eficiência reduzida

aumenta o risco de hipercalcemia e de toxicidade farmacológica secundária (i.e. digitalis). Em branco, nem Sevelamer nem lanthanum foram estudados com diuréticos, mas a hipercalcemia não é um efeito secundário.

sem interacção (demonstrado em estudos in vitro ou in vivo).

interacção não especificada.

Não descrito mas com um potencial efeito de classe.

/div>Demonstrou a ausência de interacção também com furosemida e losartan.
Aglutinantes de fosfato à base de cálcioCarbonato de cálcio (Mastical®, Caosina®)
Carbonato de cálcio pode modificar a absorção de vários fármacos, pelo que estes devem ser administrados pelo menos 2h antes ou 4-6h depois do aglutinante. Para além dos indicados, devem ser destacados outros antibióticos tais como neomicina, cloranfenicol e fosfomicina, corticosteróides sistémicos, fenitoína, barbitúricos, antiácidos contendo sais de alumínio, colestiramina, zinco, fluoretos e sais de ferro.11,12 Esta última interacção é importante para evitar combinações dos aglutinantes de fosfato à base de cálcio8 comummente utilizados com aglutinantes contendo ferro. Tal como observado com os outros ligantes, é importante lembrar que a eficácia da levothyroxina pode ser reduzida pela utilização simultânea de ligantes de cálcio. Isto significa que a administração de carbonato de cálcio e levothyroxina deve ser separada por pelo menos 4h.13
Outra interacção a ter em conta, esta de natureza farmacodinâmica, é que a hipercalcemia pode aumentar a toxicidade da digitalis (digoxina) e que os diuréticos de tiazida reduzem a excreção urinária de cálcio, pelo que existe um risco acrescido de hipercalcemia quando coadministrada com aglutinantes de fosfato contendo cálcio. Da mesma forma, o tratamento concomitante com derivados de vitamina D e/ou medicamentos ou nutrientes que contenham cálcio (leite) pode favorecer a hipercalcemia e a síndrome leite-alcalina. Além disso, a ingestão de grandes quantidades de cálcio pode causar uma precipitação de ácidos biliares e gordos sob a forma de sabões que podem alterar a absorção de ácido ursodesoxicólico e fenodesoxicólico, bem como de gorduras e vitaminas lipossolúveis.12,13
Acetato de cálcio (Royen®, RenaCare® acetato de cálcio)
Como mencionado para o carbonato de cálcio, a administração de acetato de cálcio com alguns medicamentos pode alterar a sua absorção ou favorecer a sua toxicidade através da hipercalcemia. Para além da informação apresentada no quadro, deve salientar-se o efeito pouco conhecido sobre a diminuição da eficácia dos antagonistas do cálcio.14 Apesar de um estudo farmacoepidemiológico retrospectivo se ter referido à pouca ou nenhuma interferência do acetato de cálcio na absorção de levotiroxina,15 dados recentes sugerem que os doentes hipotiróides devem ser avisados de tomar a dose de levotiroxina claramente separada de qualquer formulação com cálcio.16
A combinação acetato de cálcio/carbonato de magnésio (Osvaren®)
A combinação acetato de cálcio/carbonato de magnésio pode alterar a absorção de alguns medicamentos incluídos na tabela, pelo que não devem ser tomados em 2h antes ou 3h após a administração do aglutinante de fosfato.17 Para além da diminuição da absorção de cefuroxima, cefpodoxima ou nitrofurantoína, também é descrita a interacção com a absorção de zinco, fluoretos e a halofantrina antimalárica.17 Da mesma forma, a ingestão de magnésio pode influenciar a absorção de ferro, um suplemento comum incluído na polimedicação do doente com CKD. O acetato de cálcio/carbonato de magnésio também pode produzir hipermagnesemia, pelo que os antiácidos que contêm não só cálcio mas também sais de magnésio devem ser evitados. Os sais de magnésio podem favorecer a absorção da digoxina no tracto gastrointestinal, diminuindo a sua biodisponibilidade, para além da possibilidade de aumentar a sua potencial toxicidade devido à hipercalcemia. O resumo das características do produto desta combinação descreve a possibilidade de que a sua utilização concomitante com estrogénios possa produzir um aumento dos níveis séricos de cálcio no seio.17 Curiosamente, ao contrário dos outros aglutinantes, é mencionado que pode ocorrer um aumento na absorção de levothyroxina se administrada em combinação com hidróxido de alumínio17,18; contudo, como mencionado, dados recentes sugerem que a administração de levothyroxina deve ser claramente separada de qualquer formulação com cálcio16 e outros aglutinantes.
Aglutinantes sem cálcio: polímeros e metais
Como mostra a figura 1, o número de interacções farmacológicas descritas com aglutinantes de uma estrutura de polímero (sevelamer) ou metais (lantânio, ferro) é inferior ao dos aglutinantes de fosfato à base de cálcio. Contudo, há abundante informação sobre as interacções medicamentosas destes aglutinantes, uma vez que foram incorporados mais recentemente no arsenal terapêutico e estes fármacos tiveram de dirigir mais perguntas às agências oficiais nos seus ensaios clínicos. Salientamos que, nestes estudos, os pacientes com medicamentos antiarrítmicos ou anticonvulsivos foram especificamente excluídos. Em geral, seria também aconselhável evitar a co-administração destes medicamentos com qualquer tipo de ligantes fosfatados.
Sevelamer (Renagel®, Renvela®, genérico Sevelámero)
Sevelamer é um polímero reticulado inabsorvível. Os medicamentos que mostram uma redução da sua biodisponibilidade pelo sevelamer devem ser administrados pelo menos uma hora antes ou três horas após a administração do sevelamer.19 Estudos sobre as interacções medicamentosas em voluntários saudáveis revelaram que o cloridrato de sevelamer reduziu a biodisponibilidade da ciprofloxacina em aproximadamente 50%.20 É muito importante saber que o sevelamer pode reduzir os níveis plasmáticos de ciclosporina, tacrolimus e micofenolato mofetil em pacientes transplantados, embora sem consequências clínicas aparentes (por exemplo, rejeição do enxerto). Ainda assim, a monitorização dos seus níveis plasmáticos é aconselhável durante a utilização desta combinação e após a sua retirada. Os níveis de TSH devem ser monitorizados em doentes que recebem levothyroxina (como com qualquer ligante). O sevelamer pode diminuir a absorção de vitaminas D, E, K e ácido fólico lipossolúveis, com repercussões clínicas discutíveis.19 Pelo contrário, em voluntários saudáveis, o sevelamer não teve qualquer efeito na biodisponibilidade de medicamentos tão importantes como a digoxina, a warfarina, o enalapril ou o metoprolol.21 Contudo, a coadministração de inibidores da bomba de protões com sevelamer pode aumentar, raramente, os níveis de fosfato sérico.21
Carbonato de Lantânio (Fosrenol®)
Lantânio pode aumentar o pH gástrico (um efeito semelhante é observado com os ligantes de fosfato à base de cálcio que são frequentemente utilizados em combinações de antiácidos) e diminuir a absorção oral de fármacos alcalinos fracos. Recomenda-se não tomar estes compostos duas horas antes ou depois da administração de carbonato de lantânio (ou seja, antimaláricos como a cloroquina e a hidroxicloroquina, o agente antifúngico cetoconazol ou bisfosfonatos).22 A biodisponibilidade da ciprofloxacina oral diminuiu aproximadamente 50% quando administrada juntamente com carbonato de lantânio num estudo sobre voluntários saudáveis.23 Em contraste, o carbonato de lantânio não afectou as concentrações séricas das vitaminas lipossolúveis A, D, E e K,24 embora recentemente tenham sido descritas interacções in vitro com a vitamina K2.25 É também importante salientar que, em voluntários saudáveis, a administração de carbonato de lantânio não modificou o perfil farmacocinético da digoxina, warfarina, metoprolol, fenitoína ou enalapril.22
Exi-hidróxido de suícroferrido
Não parecido com outros ligantes fosfatados, existe informação considerável sobre a ausência de interacções de OHS com outros medicamentos (ver figura 1). Além disso, foi descrito que não há interacção relevante in vitro da SHV com cefalexina, nifedipina e quinidina, entre outros (figura 1).26 Em voluntários saudáveis não há interacções relevantes nem com losartan, furosemida, omeprazol, digoxina ou warfarina.27 A SHV não interage com estatinas (atorvastatina e sinvastatina) em doentes em diálise, apesar dos dados preliminares in vitro sugerirem a possibilidade de tal interacção. Ao contrário do sevelamer, a OHS não afecta a actividade inibitória da vitamina D oral sobre PTH28 e, ao contrário do lantânio, não parece interagir com a vitamina K2.25 Pode ser possível ver uma menor absorção oral de fármacos que interagem com o ferro (como o alendronato e a doxiciclina) ou, como os outros aglutinantes, com a levothyroxina.29
Aglutinantes à base de alumínio
Embora as directrizes do KDIGO recomendem (evidência 1C) para evitar o uso prolongado de aglutinantes de fosfato à base de alumínio,2 a figura 1 apresenta as múltiplas possibilidades de interacções, quer pela sua potencial prescrição fora do nosso âmbito, quer como uma fórmula principal.30 Devemos também destacar a possibilidade de interacções desconhecidas com imunossupressores ou medicamentos recentemente desenvolvidos.
Conclusão
Parte dos potenciais efeitos negativos descritos dos ligantes fosfatados contendo cálcio, devemos também ter em conta a maior frequência de possíveis interacções medicamentosas com muitos medicamentos usados rotineiramente nos nossos pacientes polimedicados. Em geral, outros ligantes, tais como sevelamer, lantânio e OHS provaram a ausência de interacções significativas com fármacos para os quais não existe informação disponível com os ligantes mais antigos. Do mesmo modo, deve ter-se em mente que aqueles aglutinantes que necessitam de um número menor de comprimidos em monoterapia, não só melhorarão a aderência ao tratamento, mas também diminuirão o risco de possíveis interacções indesejáveis. Em qualquer caso, embora o potencial de interacções pareça baixo para alguns ligantes, especialmente OHS, a sua utilização com fármacos com uma gama terapêutica estreita aconselharia a separar as doses para alcançar o efeito clínico e reduzir as reacções adversas, tanto no início do tratamento como após ajustamentos de dose subsequentes.
Declaração dos autores
Os autores aprovam o envio do artigo para publicação na revista Nefrologia e declaram que não foi enviado simultaneamente para qualquer outra revista para publicação. Os autores declaram também que se trata de uma ideia não originária da indústria farmacêutica e que a sua propriedade intelectual é transferida para a Nefrologia. Os autores aprovam a forma final e são responsáveis pelo seu conteúdo.
Conflitos de interesse
J.B. recebeu honorários de conferências da Abbvie, Amgen, Genzyme e Shire, e como consultor da Abbvie, Amgen, Vifor/Fresenius-Renal Pharma, Chugai, Medice e Genzyme/Sanofi. J.F.N.G. recebeu honorários de conferências e/ou consultadoria da Abbvie, Amgen, Astra-Zeneca, Boehringer-Ingelheim, Esteve, Genzyme, Sanofi, Servier, Shire e Vifor/Fresenius-Renal Pharma. M.D.A. recebeu conferências ou honorários de consultores da Shire, Fresenius, Abbvie e Amgen. E.G.P. recebeu honorários de consultores da Sanofi, Vifor/Fresenius-Renal Pharma, Amgen, Abbvie e Shire. A.L.M.F. recebeu honorários de conferências da General Electric e Astra Zeneca e honorários de consultores da Vifor/Fresenius-Renal Pharma. A E.S. recebeu honorários de Abbvie, Sanofi, Shire, Vifor/Fresenius-Renal Pharma. A.M.M. recebeu honorários de conferências da Abbvie, Amgen, Shire, Bellco, Fresenius-Medical Care. M.J.Ll. recebeu honorários de conferências da Sanofi e Abbvie, e honorários de consultores da Vifor/Fresenius-Renal Pharma. P.M.V. recebeu honorários de conferências da Amgen, Sanofi e Vifor/Fresenius-Renal Pharma e honorários de consultores da Vifor/Fresenius-Renal Pharma. M.A.B. recebeu honorários de conferências da Vifor/Fresenius-Renal Pharma. I.D. recebeu honorários por colaboração científica com Vifor/Fresenius-Renal Pharma.