danos no DNAEditar

Dano de ADN é considerado como a causa primária subjacente das neoplasias malignas conhecidas como cancros. O seu papel central na progressão para o cancro é ilustrado na figura desta secção, na caixa perto do topo (as características centrais dos danos de ADN, alterações epigenéticas e reparação deficiente do ADN na progressão para o cancro são mostradas a vermelho). Os danos no ADN são muito comuns. Os danos naturais do ADN (devidos principalmente ao metabolismo celular e às propriedades do ADN na água à temperatura corporal) ocorrem a uma taxa de mais de 60.000 novos danos, em média, por célula humana, por dia . Podem ocorrer danos adicionais no ADN devido à exposição a agentes exógenos. O fumo do tabaco causa um aumento dos danos do ADN exógeno, e estes danos do ADN são a causa provável do cancro do pulmão devido ao tabagismo. A luz UV da radiação solar causa danos no ADN que são importantes no melanoma. A infecção por Helicobacter pylori produz níveis elevados de espécies reactivas de oxigénio que danificam o ADN e contribuem para o cancro gástrico. Os ácidos biliares, a níveis elevados nos cólons humanos que ingerem uma dieta rica em gordura, também causam danos no ADN e contribuem para o cancro do cólon. Katsurano et al. indicaram que os macrófagos e neutrófilos num epitélio inflamado do cólon são a fonte de espécies reactivas de oxigénio que causam os danos do ADN que iniciam a tumorigenese do cólon. Algumas fontes de danos de ADN estão indicadas nas caixas no topo da figura desta secção.
Indivíduos com uma mutação da linha germinal que causa deficiência em qualquer um dos 34 genes de reparação de ADN (ver artigo Desordem de deficiência de reparação de ADN) estão em risco acrescido de cancro. Algumas mutações da linha germinal nos genes reparadores de ADN causam até 100% de probabilidade de cancro ao longo da vida (por exemplo, mutações p53). Estas mutações da linha germinal são indicadas numa caixa à esquerda da figura com uma seta indicando a sua contribuição para a deficiência de reparação do ADN.
Sobre 70% das neoplasias malignas não têm componente hereditário e são chamadas “cancros esporádicos”. Apenas uma minoria de cancros esporádicos tem uma deficiência na reparação do ADN devido à mutação de um gene de reparação do ADN. Contudo, a maioria dos cancros esporádicos tem uma deficiência na reparação do ADN devido a alterações epigenéticas que reduzem ou silenciam a expressão do gene reparador do ADN. Por exemplo, de 113 cancros colorrectais sequenciais, apenas quatro tinham uma mutação falsa no gene MGMT de reparação do ADN, enquanto a maioria tinha reduzido a expressão do MGMT devido à metilação da região promotora do MGMT (uma alteração epigenética). Cinco relatórios apresentam provas de que entre 40% e 90% dos cancros colorrectais reduziram a expressão do MGMT devido à metilação da região promotora do MGMT.
Similiarmente, dos 119 casos de cancros colorrectais deficientes em reparação de incompatibilidade que não tinham expressão do gene de reparação do ADN PMS2, PMS2 era deficiente em 6 devido a mutações no gene PMS2, enquanto em 103 casos a expressão PMS2 era deficiente porque o seu parceiro MLH1 foi reprimido devido à metilação do promotor (a proteína PMS2 é instável na ausência do MLH1). Nos outros 10 casos, a perda da expressão PMS2 foi provavelmente devida à sobreexpressão epigenética do microRNA, miR-155, que desregula MLH1.
Em outros exemplos, foram encontrados defeitos epigenéticos em frequências entre 13%-100% para os genes de reparação do ADN BRCA1, WRN, FANCB, FANCF, MGMT, MLH1, MSH2, MSH4, ERCC1, XPF, NEIL1 e ATM. Estes defeitos epigenéticos ocorreram em vários cancros (por exemplo, peito, ovário, colorrectal e cabeça e pescoço). Duas ou três deficiências na expressão de ERCC1, XPF ou PMS2 ocorrem simultaneamente na maioria dos 49 cancros de cólon avaliados por Facista et al. Alterações epigenéticas que causam uma expressão reduzida dos genes de reparação de ADN são mostradas numa caixa central no terceiro nível a partir do topo da figura desta secção, e a consequente deficiência de reparação de ADN é mostrada no quarto nível.
Quando a expressão dos genes de reparação de ADN é reduzida, os danos no ADN acumulam-se nas células a um nível superior ao normal, e estes danos em excesso causam um aumento da frequência de mutação ou epimutação. As taxas de mutação aumentam fortemente nas células defeituosas em reparações de DNA não compatíveis ou em reparações homólogas recombinacionais (HRR).
Durante a reparação das quebras de fios duplos de DNA, ou a reparação de outros danos de DNA, os locais de reparação incompletamente limpos podem causar silenciamento de genes epigenéticos. As deficiências de reparação do ADN (nível 4 na figura) causam um aumento dos danos no ADN (nível 5 na figura) que resultam num aumento das mutações somáticas e alterações epigenéticas (nível 6 na figura).
Defeitos de campo, tecido de aspecto normal com múltiplas alterações (e discutidos na secção abaixo), são precursores comuns do desenvolvimento do clone de tecido desordenado e que prolifera de forma imprópria numa neoplasia maligna. Tais defeitos de campo (segundo nível do fundo da figura) podem ter mutações múltiplas e alterações epigenéticas.
Após a formação de um cancro, este tem geralmente instabilidade genómica. Esta instabilidade é provavelmente devida a uma reparação reduzida do ADN ou a danos excessivos no ADN. Devido a esta instabilidade, o cancro continua a evoluir e a produzir subclones. Por exemplo, um cancro renal, amostrado em 9 áreas, teve 40 mutações ubíquas, demonstrando heterogeneidade tumoral (ou seja, presente em todas as áreas do cancro), 59 mutações partilhadas por algumas (mas não todas as áreas), e 29 mutações “privadas” presentes apenas numa das áreas do cancro.
Defeitos de campoEdit
Vários outros termos foram utilizados para descrever este fenómeno, incluindo “efeito de campo”, “cancerização de campo”, e “carcinogénese de campo”. O termo “cancerização de campo” foi usado pela primeira vez em 1953 para descrever uma área ou “campo” de epitélio que foi pré-condicionado por (nessa altura) processos largamente desconhecidos de modo a predispor o mesmo para o desenvolvimento do cancro. Desde então, os termos “cancerização de campo” e “defeito de campo” têm sido utilizados para descrever tecido pré-maligno no qual é provável que surjam novos cancros.
Defeitos de campo são importantes na progressão para o cancro. No entanto, na maioria das investigações sobre o cancro, como salientou Rubin “A grande maioria dos estudos na investigação do cancro tem sido feita sobre tumores bem definidos in vivo, ou sobre focos neoplásicos discretos in vitro. No entanto, há provas de que mais de 80% das mutações somáticas encontradas nos tumores colorrectais humanos do fenótipo mutante ocorrem antes do início da expansão clonal terminal. Da mesma forma, Vogelstein et al. salientam que mais de metade das mutações somáticas identificadas nos tumores ocorreram numa fase pré-neoplásica (num defeito de campo), durante o crescimento de células aparentemente normais. Da mesma forma, alterações epigenéticas presentes nos tumores podem ter ocorrido em defeitos de campo pré-neoplásicos.
Uma visão expandida do efeito de campo foi denominada “efeito de campo etiológico”, que abrange não só alterações moleculares e patológicas nas células pré-neoplásicas, mas também influências de factores ambientais exógenos e alterações moleculares no microambiente local na evolução neoplásica desde o início do tumor até à morte do paciente.
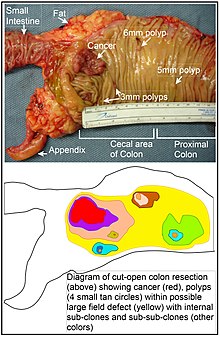
No cólon, um defeito de campo surge provavelmente pela selecção natural de uma célula mutante ou epigenicamente alterada entre as células estaminais na base de uma das criptas intestinais na superfície interna do cólon. Uma célula estaminal mutante ou epigenéticamente alterada pode substituir as outras células estaminais próximas por selecção natural. Assim, pode surgir uma mancha de tecido anormal. A figura nesta secção inclui uma fotografia de um segmento do cólon recentemente ressecado e aberto ao comprimento, mostrando um cancro do cólon e quatro pólipos. Abaixo da fotografia, há um diagrama esquemático de como uma grande mancha de células mutantes ou epigeneticamente alteradas pode ter-se formado, mostrado pela grande área em amarelo no diagrama. Dentro desta primeira grande mancha no diagrama (um grande clone de células), uma segunda tal mutação ou alteração epigenética pode ocorrer para que uma determinada célula estaminal adquira uma vantagem em comparação com outras células estaminais dentro da mancha, e esta célula estaminal alterada pode expandir clonalmente formando uma mancha secundária, ou subclone, dentro da mancha original. Isto é indicado no diagrama por quatro pequenas manchas de cores diferentes dentro da grande área original amarela. Dentro destes novos remendos (subclones), o processo pode ser repetido várias vezes, indicado pelos remendos ainda mais pequenos dentro dos quatro remendos secundários (com cores ainda diferentes no diagrama) que se expandem clonalmente, até que surjam células estaminais que geram ou pequenos pólipos ou então uma neoplasia maligna (cancro).
Na fotografia, um aparente defeito de campo neste segmento de um cólon gerou quatro pólipos (rotulados com o tamanho dos pólipos, 6mm, 5mm, e dois de 3mm, e um cancro de cerca de 3 cm de largura na sua dimensão mais longa). Estas neoplasias são também indicadas, no diagrama abaixo da fotografia, por 4 pequenos círculos bronzeados (pólipos) e uma área vermelha maior (cancro). O cancro na fotografia ocorreu na área cecal do cólon, onde o cólon se junta ao intestino delgado (rotulado) e onde ocorre o apêndice (rotulado). A gordura na fotografia é externa à parede exterior do cólon. No segmento de cólon aqui mostrado, o cólon foi aberto longitudinalmente para expor a superfície interna do cólon e para mostrar o cancro e os pólipos que ocorrem no interior do revestimento epitelial interno do cólon.
Se o processo geral pelo qual surgem os cancros esporádicos do cólon é a formação de um clone pré-neoplástico que se espalha por selecção natural, seguido da formação de subclones internos dentro do clone inicial, e subclones dentro destes, então os cancros do cólon devem geralmente ser associados a, e ser precedidos por, campos de anormalidade crescente reflectindo a sucessão de eventos pré-malignos. A região mais extensa de anomalia (a área irregular amarela mais externa no diagrama) reflectiria o acontecimento mais precoce na formação de uma neoplasia maligna.
Na avaliação experimental de deficiências específicas de reparação de ADN em cancros, também se mostrou que muitas deficiências específicas de reparação de ADN ocorrem nos defeitos de campo que envolvem esses cancros. A Tabela, abaixo, dá exemplos em que se demonstrou que a deficiência de reparação de ADN num cancro foi causada por uma alteração epigenética, e as frequências um pouco mais baixas com que a mesma deficiência de reparação de ADN epigenética foi encontrada no defeito de campo circundante.
| Cancer | Ref. | |||
|---|---|---|---|---|
| Colorectal | MGMT | 46% | 34% | /td>> |
| Colorectal | MGMT | 47% | 11% | |
| Colorectal | MGMT | 70% | 60% | |
| Colorectal | MSH2 | 13% | 5% | |
| Colorectal | ERCC1 | 100% | 40% | |
| PMS2 | 88% | 50% | /td> | XPF | 55% | 40% |
| Head and Neck | MGMT | 54% | 38% | |
| Head and Neck | MLH1 | 33% | 25% | >/td>>/td> |
| Head and Neck | MLH1 | 31% | 20% | |
| Stomach | MGMT | 88% | 78% | |
| Stomach | MLH1 | 73% | 20% | >/td> |
| Esophagus | MLH1 | 77%-100% | 23%-79% |
alguns dos pequenos pólipos no defeito de campo mostrado na foto do segmento de cólon aberto podem ser neoplasias relativamente benignas. Dos pólipos de tamanho inferior a 10mm, encontrados durante a colonoscopia e seguidos de colonoscopias repetidas durante 3 anos, 25% permaneceram inalterados em tamanho, 35% regrediram ou encolheram em tamanho enquanto 40% cresceram em tamanho.
Instabilidade do genomaEdit
Cancers são conhecidos por exibirem instabilidade do genoma ou um fenótipo mutante. O ADN codificador de proteínas dentro do núcleo é cerca de 1,5% do ADN genómico total. Dentro deste ADN codificador de proteínas (chamado exoma), um cancro médio da mama ou do cólon pode ter cerca de 60 a 70 mutações alteradoras de proteínas, das quais cerca de 3 ou 4 podem ser mutações “condutoras”, e as restantes podem ser mutações “passageiros” No entanto, o número médio de mutações de sequência de ADN em todo o genoma (incluindo regiões não codificadoras de proteínas) dentro de uma amostra de tecido canceroso da mama é de cerca de 20.000. Numa amostra média de tecido de melanoma (onde os melanomas têm uma frequência de mutação exoma mais elevada) o número total de mutações de sequência de ADN é de cerca de 80.000. Isto é comparável à frequência muito baixa de mutação de cerca de 70 novas mutações em todo o genoma entre gerações (de pais para filhos) em humanos.
As altas frequências de mutações nas sequências totais de nucleótidos dentro dos cancros sugerem que muitas vezes uma alteração precoce nos defeitos de campo que dão origem a um cancro (por exemplo, área amarela no diagrama desta secção) é uma deficiência na reparação do ADN. Os grandes defeitos de campo à volta dos cancros do cólon (estendendo-se até cerca de 10 cm de cada lado de um cancro) foram mostrados por Facista et al. como tendo frequentemente defeitos epigenéticos em 2 ou 3 proteínas de reparação de ADN (ERCC1, XPF ou PMS2) em toda a área do defeito de campo. Deficiências na reparação do ADN causam taxas de mutação aumentadas. Uma deficiência na reparação do ADN, por si só, pode permitir a acumulação de danos no ADN, e a síntese de translação propensa a erros, para além de alguns desses danos, pode dar origem a mutações. Além disso, a reparação defeituosa destes danos acumulados no ADN pode dar origem a epimutações. Estas novas mutações ou epimutações podem fornecer uma vantagem proliferativa, gerando um defeito de campo. Embora as mutações/epimutações nos genes de reparação do ADN não conferem, elas próprias, uma vantagem selectiva, podem ser transportadas como passageiros em células quando as células adquirem mutações/epimutações adicionais que proporcionam uma vantagem proliferativa.