Objectivo de Aprendizagem
1. Identificar os grupos funcionais aldeído, cetona, ácido, éster, e éter.
2. Utilizar convenções de denominação adequadas para aldeído, cetona, ácido carboxílico, e moléculas contendo éster e éter.
Existem outros grupos funcionais que contêm átomos de oxigénio. Um grupo carbonilo é formado quando um átomo O e um átomo C são unidos por uma dupla ligação. Neste diagrama, o grupo R representa qualquer cadeia de hidrocarbonetos:
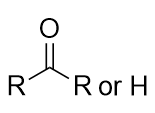
Se uma ligação do grupo carbonilo for feita a um átomo de hidrogénio, então a molécula é ainda classificada como um aldeído. Ao nomear aldeídos, a cadeia principal dos átomos C deve incluir o carbono no grupo carbonilo, que é numerado como posição 1 na cadeia do carbono. É utilizado o nome de origem do hidrocarboneto, mas o sufixo -al é anexado. (Não confundir -al com -ol, que é o sufixo utilizado para os álcoois.) Assim, temos
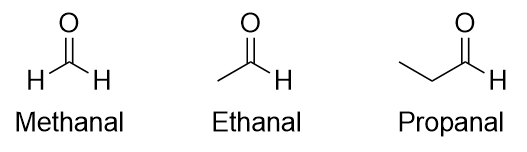
Methanal tem um nome comum com o qual se pode estar familiarizado: formaldeído. O principal aspecto a notar sobre os aldeídos é que o grupo carbonilo está no fim de uma cadeia de carbono.
Um grupo carbonilo no meio de uma cadeia de carbono implica que ambas as ligações remanescentes do grupo carbonilo são feitas aos átomos C. Este tipo de molécula é chamado de cetona. Apesar de aldeídos e cetonas terem o mesmo grupo carbonilo, têm propriedades químicas e físicas diferentes e estão devidamente agrupados como dois tipos diferentes de compostos. A cetona mais pequena tem três átomos de C. Ao nomear uma cetona, tomamos o nome do hidrocarboneto pai e alteramos o sufixo para -one:

O nome comum para propanona é acetona. Com cetonas maiores, devemos usar um número locante para indicar a posição do grupo carbonilo imediatamente antes do sufixo, como fizemos com alcenos e alcinos:
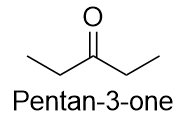
Há uma forma não IUPAC de nomear cetonas que também é comummente usada: nomear os grupos alquilo que estão ligados ao grupo carbonilo e adicionar a palavra cetona ao nome. Assim, propanona também pode ser chamada de dimetilcetona, enquanto butano-2-ona é chamada de metiletilcetona.
Exemplo 9
Desenhar a estrutura de pentano-2-one.
Solução
Esta molécula tem cinco átomos de C numa cadeia, com o grupo carbonilo no segundo átomo de C. A sua estrutura é:
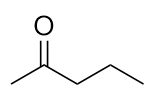
Teste-te a ti mesmo
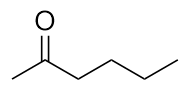
Desenhar a estrutura de metilbutilcetona.
Resposta
/div>
A combinação de um grupo funcional carbonil e um grupo hidroxil faz o grupo carboxil.

Molecules com um grupo carboxil são chamados ácidos carboxílicos. Tal como no caso dos aldeídos, o grupo funcional em ácidos carboxílicos encontra-se no fim de uma cadeia de carbono. Também como com os aldeídos, o átomo C no grupo funcional é contado como um dos átomos C que define o nome do hidrocarboneto pai. Para designar os ácidos carboxílicos, utiliza-se o nome parental do hidrocarboneto, mas o sufixo – ácido oleico é adicionado:

Ácido metanóico e ácido etanóico são também chamados ácido fórmico e ácido acético, respectivamente. O ácido fórmico é o composto que faz picadas de formigas, enquanto que o ácido acético é a substância activa no vinagre.
Como ácidos são os ácidos carboxílicos? Acontece que eles não são muito ácidos. Nenhum ácido carboxílico está na lista de ácidos fortes (Tabela 12.2 “Ácidos e Bases Fortes”). (Para mais informações sobre ácidos fortes, ver Secção 12.4 “Ácidos e Bases Fortes e Fracos e os seus Sais”). Isto significa que todos os ácidos carboxílicos são ácidos fracos. Uma solução de 1 M de ácido fórmico é apenas cerca de 1,3% dissociada em iões H+ e iões formados, enquanto uma solução semelhante de ácido acético é ionizada por cerca de apenas 0,4%. Alguns ácidos carboxílicos são mais fortes – por exemplo, o ácido tricloroacético é cerca de 45% dissociado em solução aquosa. Mas nenhum ácido carboxílico se aproxima da quantidade de dissociação de 100% requerida pela definição de um ácido forte.
Como o seu nome sugere, contudo, os ácidos carboxílicos actuam como ácidos na presença de bases. O átomo H no grupo carboxílico sai como o ião H+, deixando um ião carboxilato:

iões carboxilato são nomeados pelo nome ácido: o ácido -oico é substituído por -oate para nomear o ião.
Exemplo 10
Completar a reacção química. É possível nomear o ião carboxilato formado?

Solução
O ião OH- remove o átomo H que faz parte do grupo carboxil:

O ião carboxil, que tem a fórmula estrutural condensada CH3CO2-, é o ião etanoato, mas é vulgarmente chamado ião acetato.
Teste-te a ti mesmo
Completar a reacção química. Pode nomear o ião carboxiato formado?

Resposta

O ião é o ião metanoato, que é vulgarmente chamado de ião formado.
Uma reacção a considerar é a de um ácido carboxílico e de um álcool. Quando combinado nas condições adequadas, uma molécula de água será removida, e as peças restantes serão combinadas para formar um novo grupo funcional – o grupo éster:

Nota como a molécula ácida contribui com um lado alquilo (representado por R), enquanto o álcool contribui com o outro lado (representado por R′). Os ésteres são nomeados utilizando o nome do grupo alquil do álcool mais o nome do carboxilato do ácido – por exemplo, esta molécula chama-se propanoato de metilo.
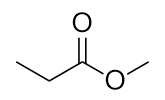 metil_propanoato
metil_propanoato
A química está em todo o lado: Ésteres, Fragrâncias, e Aromas
Esteres são compostos muito interessantes, em parte porque muitos têm odores e sabores agradáveis. (Lembre-se, nunca prove nada no laboratório de química!) Muitos ésteres ocorrem naturalmente e contribuem para a fragrância das flores e o sabor dos frutos. Outros ésteres são sintetizados industrialmente e são adicionados a produtos alimentares para melhorar o seu cheiro ou sabor. É provável que se se comer um produto cujos ingredientes incluam aromas artificiais, esses aromas sejam ésteres. Aqui estão alguns ésteres e as suas utilizações, graças aos seus odores, sabores, ou ambos:
| Ester | Ester | Tastes/Smells Like | ||
|---|---|---|---|---|
| allyl hexanoato | abacaxi | formato de isobutilo | raspberry | |
| benzyl acetato | honey | |||
| etil butanoato | banana | nonyl caprylate | orange | |
| hexanoato de etilo | abacaxi | acetato de pentilo | apple | |
| etil heptanoato | apricot | propyl ethanoate | pear | |
| ethyl pentanoate | apple | propyl isobutyrate | rum |
Finalmente, o grupo funcional é um átomo O que está ligado a dois grupos orgânicos:
R-O-R′
Os dois grupos R podem ser o mesmo ou diferente. A nomeação de éteres é como a forma alternativa de nomear cetonas. Neste caso, os grupos R são nomeados sequencialmente, e a palavra éter é anexada. A molécula CH3OCH3 é éter dimetílico, enquanto CH3OCH2CH3 é éter etílico metílico. O éter dietílico, outro éter, foi outrora utilizado como anestésico, mas a sua inflamabilidade e toxicidade fizeram com que caísse em desgraça. Moléculas mais pequenas de éter que são líquidas à temperatura ambiente são solventes comuns para reacções químicas orgânicas.
Key Takeaways
- Aldeídos, cetonas, ácidos carboxílicos, ésteres, e éteres têm grupos funcionais contendo oxigénio.
- IUPAC nome pode ser usado para aldeídos, cetonas, ácido carboxílico, e moléculas contendo ésteres e éteres.
Exercicios
-
Nomear uma semelhança entre os grupos funcionais encontrados em aldeídos e cetonas. Pode nomear uma diferença entre eles?
Explicar como um ácido carboxílico é utilizado para fazer um éster.
-
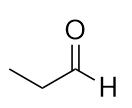
Nome cada molécula.
a)
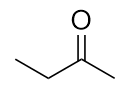
b)
-
Nome de cada molécula.
a)
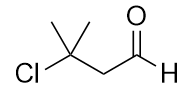
b)
-
Nome de cada molécula.
a)
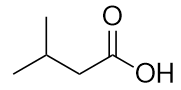
b)
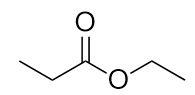
-
Nome de cada molécula.
a)
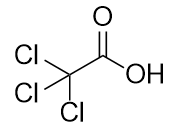
b)
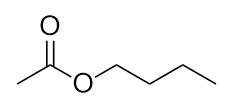
-
Nome desta molécula.
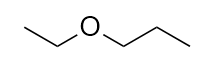
Nome desta molécula.
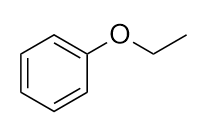
Dê um nome alternativo mas aceitável à molécula no Exercício 4.2.
Completar esta reacção química.
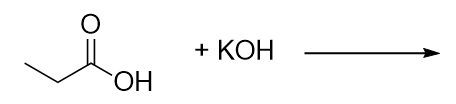
Completar esta reacção química.
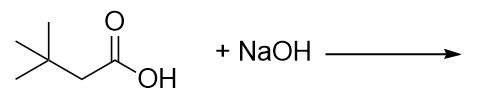
O fármaco conhecido como aspirina tem esta estrutura molecular:
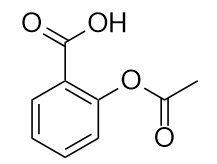
Identificar o(s) grupo(s) funcional(ais) nesta molécula.
O fármaco conhecido como naproxen sódio é o sal de sódio desta molécula:
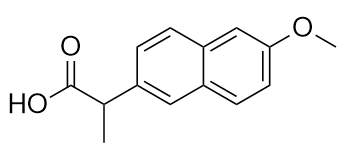
Identificar o(s) grupo(s) funcional(ais) nesta molécula.
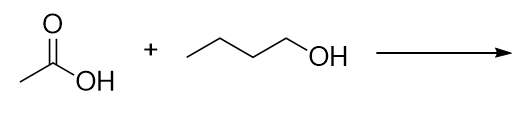
Identificar o éster feito através da reacção destas moléculas.
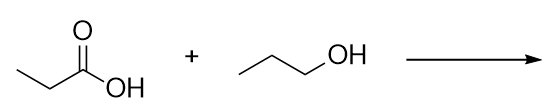
Identificar o éster feito reagindo a estas moléculas.
Respostas
1. Ambos têm um grupo carbonilo, mas um aldeído tem o grupo carbonilo no fim de uma cadeia de carbono, e o carbono carbonilo de uma cetona está rodeado por dois outros carbonos.
a) propanal
b) butan-2-one
a) ácido 3-metilbutanóico
b) propionato de etilo
7. éter etil propílico
9. etilcetona
11. H2O + KCH3CH2CO213. ácido, éster, e aromático (anel de benzeno)
15. propionato de propilo