As Doenças de Motilidade Esofágica são frequentemente uma condição negligenciada. Não só as apresentações clínicas não específicas tais como, azia, dor no peito e tosse crónica se sobrepõem frequentemente às outras doenças comuns, como também há falta de equipamento para testar a função esofágica.
Função motora esofágica usada para ser avaliada pela manometria convencional exibindo os resultados em traçado de linha. Em 2001, Spechler e Castell1 propuseram a aplicação destes dados para classificar as doenças manométricas esofágicas em 4 grupos:
1. Relaxamento esofágico inferior inadequado (LES) que pode ser acalasia clássica ou perturbações atípicas do relaxamento LES.
2. Contracção corporal esofágica não coordenada referente a espasmo esofágico difuso.
3. Hipercontracção esofágica que pode ocorrer no corpo (esófago quebra-nozes) ou LES (LES hipertensivo).
4. hipocontracção do corpo esofágico que significa motilidade esofágica ineficaz (IEM).
Em 1991, Clouse et al,2 começaram a criar parcelas topográficas esofágicas a partir de um estudo manométrico convencional, e revelaram maior precisão diagnóstica para a dismotilidade esofágica.3 Durante a reunião do DDW de 2007 em San Diego, o grupo de trabalho de manometria de alta resolução (HRM) frst colaborou para ajustar a topografia de pressão esofágica (EPT) para avaliar a dismotilidade clínica do esófago. Em 2008, Kahrilas et al.4 publicaram a primeira classificação de Chicago (CC) utilizando a topografia de pressão esofágica para o diagnóstico da dismotilidade esofágica, e mais tarde, em 2012 e 2015, foram anunciadas as versões CC 2.0 e 3.0, respectivamente.5,6
De acordo com a versão CC 3.0, a dismotilidade esofágica é principalmente classificada em;
1. LES pouco relaxante que poderia ser acalasia ou esofagogástrico
junção (EGJ) outflow obstrução.
2. Principais perturbações do peristaltismo: ausência de contractilidade, esofágica distal
espasmo ou esófago de martelo pneumático e
3. Pequenas perturbações do peristaltismo: IEM ou peristaltismo fragmentado.6
Hypotensive (end expiratory resting LES pressure < 10 mmHg com peristaltismo normal) e LES hipertensivo (end expiratory resting LES > 35 mmHg com peristaltismo normal e relaxação EGJ) ambos mencionados na versão CC 1.04 não é emitido na versão 2.0 e 3.0.5, 6 Cada distúrbio de motilidade esofágica como mencionado no CC versão 3.0 será revisto neste artigo.
Achalasia
A acalasia idiopática é um distúrbio esofágico primário caracterizado pela perda de peristaltismo esofágico e diminuição do relaxamento LES.7 Aproximadamente 3-4% dos doentes com suspeita de acalasia serão pseudoacalasia,8 uma condição que ocorre quando células malignas estão a inflar e a destruir o plexo mioentérico do esófago distal ou EGJ. A acalasia idiopática é uma doença rara. A incidência é de 0,3-1,63 por 100.000 adultos por ano,9-13 e a prevalência é de 8,7-11,2 por 100.000 adultos em 10 anos,9,13,14
Patogénese de acalasia é a função prejudicada ou perda de neurónios inibidores pós-ganglionares no plexo mirínico, que fornecem músculo liso do esófago distal e EGJ, secretando dois neurotransmissores: o polipéptido intestinal vasoactivo (VIP) e o óxido nítrico (NO).15, 16 Todos estes, em conjunto, conduzem à abertura esofágica e a um LES pouco relaxante.17 Linfócitos citotóxicos e/ou activação do complemento podem causar este ganglionite crónico, especialmente em doentes com alelos HLA DQA1*0103 e HLA DQB1*0603.18 Alguns vírus, por exemplo, o vírus do herpes simplex-1 (HSV-1), sarampo, papilomavírus humano (HPV) e o vírus da varicela zoster (VZV) foram hipotéticos de estarem envolvidos na patogénese da acalasia idiopática. Contudo, nenhum estudo defendeu frmly esta associação.17, 19 As manifestações clínicas da acalasia idiopática presumivelmente correlacionam-se com o grau de patologia do esófago. Inicialmente, os doentes com neurite mioentérica esofágica ou ganglionite estão predominantemente presentes com acalasia vigorosa (acalasia tipo III). Posteriormente, quando o processo inflammatory resultar numa perda de células ganglionares e fbroses neurais, os doentes desenvolverão acalasia clássica (tipo I) ou acalasia com compressão (tipo II).17
Mais de 90% dos doentes com acalasia presentes com disfagia de sólidos e líquidos. Outros sintomas são azia, regurgitação de alimentos não digeridos, dores no peito não cardíacas e perda de peso. Além disso, sintomas respiratórios, tais como rouquidão, dor de garganta, tosse e aspiração pulmonar também podem ser encontrados em doentes com acalasia.19, 20 A esofagogastroduodenoscopia (EGD) deve ser realizada em doentes com disfagia para excluir obstrução mecânica; contudo, a sensibilidade é baixa para o diagnóstico de acalasia, especialmente na fase inicial.19 Os fndings de EGD que podem ser encontrados na acalasia são esôfago dilatado ou tortuoso, alimentos retidos na luz esofágica, candidíase esofágica e alguma resistência ao passar o endoscópio pelo EGJ.20
Esofagografia de bário também tem baixa sensibilidade para determinar a fase inicial da acalasia. A dilatação esofágica e o aspecto de bico de pássaro podem ser encontrados na acalasia idiopática. Cautelosamente, se o comprimento do estreitamento distal do esófago for superior a 3,5 cm e a dilatação proximal do esófago for inferior a 4 cm, o médico deve suspeitar de pseudoacalasia.21
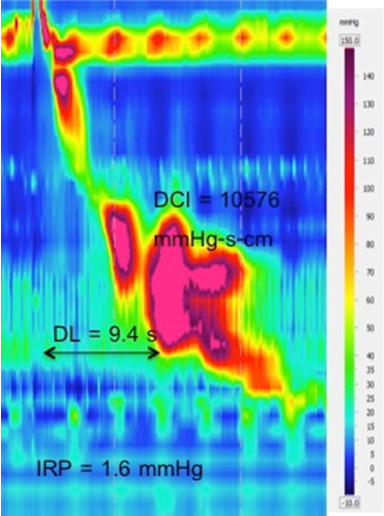
De acordo com a actual versão CC 3.0, a acalasia está classificada em 3 tipos. O critério de diagnóstico da acalasia de tipo I é o relaxamento do EGJ com 100% de peristaltismo falhado (Figura 7). A peristalase fragmentada é condição que apresenta pelo menos 50% de contracção fragmentada (uma andorinha com DCI > 450 mmHg-s-cm e quebra > 5 cm de comprimento no contorno isobárico de 20-mmHg) (Figura 7).6 Todas estas perturbações de hipomotilidade esofágica devem ter normalmente um LES.
Actualmente, a gestão da hipocontracção esofágica para a recuperação do peristaltismo esofágico é ainda limitada. O tratamento actual visa lidar com a concomitância de GERD, que é normalmente encontrada nesta doença de motilidade.69 A modificação do estilo de vida pode aumentar o trânsito do bolo esofágico, e reduzir a exposição ao ácido esofágico.69 Mastigar bem os alimentos, consumir alimentos líquidos e semi-sólidos, beber muita água e utilizar bebidas carbonatadas pode defender o trânsito do bolo esofágico e prevenir a retenção do bolo.69 A redução do peso, evitar a posição imediata de repouso após as refeições, a elevação da cabeça da cama, a posição de decúbito lateral esquerdo e evitar alimentos oleosos ou dietas de alto teor calórico podem ajudar a reduzir a exposição ao ácido esofágico e/ou a frequência dos sintomas reflux.78, 79 Além disso, há vários estudos que mostram que a mastigação de pastilhas pode diminuir a exposição ao ácido esofágico e aliviar os sintomas reflux em doentes com GERD.80-82
Tratamento farmacológico em doentes com hipocontracção esofágica consiste em terapia de supressão de ácido, alginato formando jangadas intra-gástricas inibindo tanto ácido como não ácido refluxes, e procinética como a domperidona, metoclopramida, macrólidos e agonista e/ou antagonista do receptor de serotonina.69 A fundoplicação é um tratamento eficaz a longo prazo para prevenir a gastroesofágica reflux. Embora os doentes com hipomotilidade esofágica grave devam ser cautelosos para esta cirurgia, esta condição não é uma contra-indicação absoluta.83 Além disso, há provas de que a fundoplicação pode melhorar a função esofágica em doentes com DRGE e hipomotilidade esofágica.84,85
Em conclusão, as perturbações da motilidade esofágica, incluindo a disfunção LES e a anomalia peristáltica esofágica são condições importantes. No entanto, são frequentemente subdiagnosticadas porque algumas apresentações clínicas se sobrepõem à DRGE, que se encontra mais frequentemente na prática diária. Além disso, a manometria esofágica não está amplamente disponível e os médicos em geral podem não estar familiarizados com este teste avançado da função esofágica. Mais investigação com a manometria esofágica em doentes com sintomas esofágicos refractários (tais como azia, regurgitação e dores não cardíacas no peito) e/ou sintomas respiratórios (tais como, tosse crónica) de causas pouco claras pode revelar o distúrbio único de dismotilidade esofágica. Isto poderia orientar os clínicos a escolher o tratamento adequado para os seus pacientes.