US Pharm. 2020;45(4):21-28.
ABSTRACT : Les voyageurs américains qui visitent ou travaillent dans d’autres parties du monde doivent se protéger contre les virus qui peuvent être transmis par les animaux ou les humains. Ces virus comprennent l’encéphalite japonaise, la fièvre typhoïde, la fièvre jaune, la polio, la rage et l’hépatite A. L’examen de ces maladies évitables par la vaccination permettra au pharmacien d’améliorer ses connaissances sur les mesures préventives appropriées à prendre pour éviter la maladie. Les mesures préventives comprennent le lavage élémentaire des mains, le choix approprié des vêtements pour les activités dans les zones à risque et les vaccins. Les pharmaciens sont en première ligne pour fournir des conseils aux patients et aider les voyageurs à déterminer quels vaccins sont nécessaires pour prévenir les maladies.
La récente épidémie mondiale du nouveau coronavirus 2019 SRAS-CoV-2 (connu sous le nom de coronavirus 2019 ) a amené l’Organisation mondiale de la santé (OMS) à déclarer une urgence mondiale. À l’heure actuelle, il n’existe aucun vaccin capable de protéger contre le COVID-19 ; toutefois, des efforts de développement d’un vaccin sont en cours. La prise de conscience de cette pandémie doit alerter les individus pour qu’ils se protègent des maladies évitables par la vaccination lors de leurs voyages.
Selon le CDC, il est conseillé aux voyageurs de se protéger avec des vaccins au moins 4 à 6 semaines avant le voyage. Cela laisse le temps à l’individu de développer une immunité au vaccin. Le site Web du CDC consacré à la santé des voyageurs contient des informations complètes et permet aux utilisateurs d’entrer une destination de voyage spécifique pour déterminer les vaccins et les précautions recommandés pour cette région.1 Le Comité consultatif sur les pratiques de vaccination (ACIP) fournit des recommandations et des directives concernant les vaccins utilisés pour prévenir la propagation des maladies aux États-Unis.2
Encéphalite japonaise
Vue d’ensemble : Le virus de l’encéphalite japonaise (JEV), que l’on trouve en Asie et dans le Pacifique occidental, appartient au genre Flavivirus et est étroitement lié aux virus de la fièvre jaune, du Nil occidental et de la dengue.3 Le JEV se propage par les moustiques et non par contact interhumain.3,4 Le risque d’incidence est faible mais peut varier en fonction de la saison, des activités et de la durée du voyage.5
Symptômes : Les symptômes initiaux de présentation peuvent consister en une légère fièvre ou un mal de tête, suivis d’une progression vers une maladie grave. Les symptômes de la progression comprennent l’apparition rapide d’une forte fièvre, la désorientation, les maux de tête, la raideur de la nuque, le coma, les convulsions et la paralysie spastique, et la mort peut s’ensuivre. Chez les enfants, les premiers symptômes peuvent être des douleurs gastro-intestinales et des vomissements. La période d’incubation est de 4 à 14 jours. Les personnes présentant les symptômes de la maladie ont un taux de létalité de 20 à 30 %. Les patients qui survivent au VJE subissent des répercussions tout au long de leur vie, comme une paralysie, une incapacité à parler, des crises récurrentes et d’autres conséquences intellectuelles ou neurologiques.3-5
Diagnostic : Afin d’exclure d’autres causes d’encéphalite, l’OMS recommande de rechercher les immunoglobulines M (IgM) spécifiques du VJE à l’aide d’un échantillon de liquide céphalorachidien (LCR) ou de sérum. Le prélèvement de LCR réduit les taux de faux positifs dus à une infection ou une vaccination antérieure.4
Prévention : À l’heure actuelle, il n’existe pas de traitement antiviral contre le VJE et les patients sont pris en charge par des soins symptomatiques.4 L’ACIP recommande le vaccin contre le VJE (Ixiaro) aux voyageurs passant 1 mois ou plus dans des zones endémiques, notamment les zones agricoles rurales d’Asie et les zones contenant un grand nombre de moustiques vecteurs lors de la production et de l’irrigation par inondation. Le vaccin est également recommandé pour les travailleurs de laboratoire qui risquent d’être exposés au VJE. L’ACIP ne recommande pas la vaccination systématique des voyageurs visitant des zones urbaines ou de ceux dont le séjour est inférieur à 1 mois, sauf si le voyageur prévoit des activités qui augmenteront le risque d’exposition, comme le camping ou la randonnée.5 Voir le TABLEAU 1 pour la posologie du vaccin contre l’EJ et les considérations particulières.6
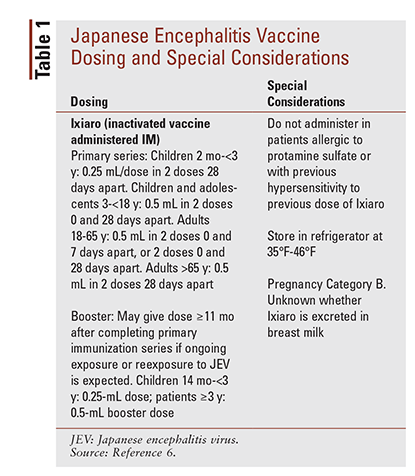
Effets indésirables : Certains effets indésirables d’Ixiaro sont des effets indésirables locaux et systémiques, des maux de tête, une maladie flulique, de la fatigue et des myalgies. Chez les enfants, les effets secondaires courants sont les convulsions fébriles et la pneumonie.6
Fièvre typhoïde
Vue d’ensemble : La fièvre typhoïde est répandue dans de nombreuses régions des Caraïbes, de l’Asie de l’Est et du Sud-Est, de l’Afrique et de l’Amérique centrale et du Sud, mais elle est peu fréquente aux États-Unis. La fièvre typhoïde et la fièvre paratyphoïde sont causées par les sérotypes Salmonella typhi et paratyphi, respectivement7. La bactérie peut se propager lorsque les excréments d’une personne infectée contaminent les aliments ou l’eau et lorsque les aliments sont préparés par une personne qui ne se lave pas les mains avant de les manipuler.8 Lorsqu’un aliment ou une boisson contaminés sont ingérés, la bactérie peut se multiplier et se propager dans la circulation sanguine, entraînant la fièvre typhoïde.9
Symptômes : Les symptômes de la typhoïde comprennent la fatigue, la faiblesse, la perte d’appétit, une forte fièvre de longue durée, une éruption cutanée (taches plates et roses), des douleurs d’estomac, de la diarrhée, de la constipation ou de la toux. Les gens peuvent, sans le savoir, transmettre la typhoïde à d’autres personnes même lorsque leurs symptômes ont disparu.8,9
Diagnostic : l’hémoculture est la principale méthode de diagnostic de la typhoïde. Des échantillons de selles, d’urine ou de moelle osseuse peuvent également être utilisés pour le diagnostic de la typhoïde ou de la paratyphoïde. Le test le plus sensible pour Salmonella typhi est la culture de moelle osseuse.10
Prévention : Le vaccin contre la typhoïde peut prévenir la fièvre typhoïde, qui peut être mortelle. La fièvre peut durer des semaines voire des mois si des antibiotiques ne sont pas pris. Environ 30% des personnes qui ne sont pas traitées meurent de complications de la fièvre typhoïde. Il existe moins d’options de traitement antibiotique car les bactéries typhoïdes résistantes aux médicaments sont devenues plus courantes dans de nombreuses régions du monde.11
Les patients peuvent être porteurs de Salmonella typhi ou paratyphi même en l’absence de symptômes. Les bactéries peuvent être transmises à d’autres personnes et la maladie pourrait revenir, c’est pourquoi un médecin doit effectuer un bilan diagnostique pour déterminer si le patient peut retourner au travail ou à l’école. Pour réduire les risques de transmission des bactéries à d’autres personnes, les patients doivent terminer le traitement antibiotique recommandé, se laver les mains avec de l’eau et du savon après avoir utilisé les toilettes et éviter de préparer et de servir de la nourriture à d’autres personnes11.
Le vaccin contre la typhoïde (Vivotif, Typhim Vi) est recommandé pour les personnes présentant un risque élevé d’exposition à la bactérie typhoïde, comme les travailleurs de laboratoire, les personnes en contact étroit avec une autre personne infectée et celles qui voyagent en Afrique, en Asie ou en Amérique centrale et du Sud12. Voir le TABLEAU 2 pour les recommandations de dosage du vaccin contre la typhoïde et les considérations particulières.13,14

Effets indésirables : Les effets indésirables de Typhim Vi, y compris la douleur, les maux de tête, la fièvre et la rougeur ou l’enflure au site d’injection, sont habituellement légers et disparaissent en quelques jours. Les effets indésirables courants de Vivotif comprennent la fièvre ou les maux de tête ; les effets secondaires moins courants sont les vomissements, les douleurs d’estomac et les éruptions cutanées. Il est rare que l’un ou l’autre vaccin entraîne des effets indésirables graves.8
Fièvre jaune
Aperçu : La fièvre jaune, qui est causée par des virus à ARN du genre Flavivirus, est apparentée au JEV, au virus du Nil occidental et à l’encéphalite de Saint-Louis. Le virus de la fièvre jaune est transmis aux humains et aux primates non humains par les animaux, principalement par les moustiques femelles Aedes aegypti qui piquent le jour et les moustiques du genre Haemagogus.15 Des précautions contre le virus de la fièvre jaune doivent être prises par les personnes voyageant en Afrique et en Amérique du Sud.16
Symptômes : La plupart des patients infectés par la fièvre jaune sont asymptomatiques ou présentent quelques symptômes légers. La période d’incubation se produit environ 3 à 6 jours avant que les symptômes ne se manifestent. Les symptômes initiaux, qui comprennent des courbatures, des frissons, des maux de tête sévères, des nausées, des vomissements, une fièvre soudaine, des douleurs dorsales, une faiblesse et une fatigue, durent généralement environ une semaine, mais parfois la fatigue et la faiblesse persistent pendant des mois. Une personne sur sept qui développe les premiers symptômes connaît une brève rémission de quelques heures ou d’un jour avant d’évoluer vers des symptômes plus graves, notamment une forte fièvre, des saignements, un choc, une jaunisse, une défaillance de plusieurs organes et la mort. Environ 30 à 60 % des patients qui développent des symptômes graves mourront.15,17
Diagnostic : Pour diagnostiquer la fièvre jaune, un échantillon de sérum est analysé en laboratoire. Des IgM spécifiques au virus et des anticorps neutralisants sont retrouvés dans le sérum des patients infectés par la fièvre jaune. Le professionnel de santé recueille également des informations sur les dates et les lieux où le patient a voyagé, les activités pratiquées pendant le voyage et les caractéristiques cliniques afin de poser un diagnostic.18
Prévention : Le vaccin contre la fièvre jaune (YF-VAX) est une forme vivante et affaiblie du virus administrée en une seule injection.17 Les personnes infectées sont probablement immunisées contre toute infection future. L’ACIP n’exige pas actuellement de vaccins de rappel, en raison de l’immunité durable conférée par une seule vaccination.19 Les voyageurs doivent consulter le site Web des CDC pour déterminer si le vaccin YF-VAX est nécessaire.1 Certains pays exigent un certificat de vaccination avant d’autoriser l’entrée dans le pays.20 Le voyageur doit recevoir une dérogation si la vaccination est contre-indiquée pour une raison médicale, mais c’est au pays de destination de déterminer si l’entrée est autorisée. Voir le TABLEAU 3 pour la posologie du YF-VAX et les considérations particulières.20,21 En outre, voici les mesures préventives que les voyageurs devraient prendre pour éviter les piqûres de moustiques pendant la journée18:
– Vaporiser ou prétremper la couche extérieure des vêtements et de l’équipement avec de la perméthrine.
– Porter des vêtements à manches longues, respirants et de couleur neutre.
– Appliquer un écran solaire, attendre 20 minutes, puis appliquer un insectifuge.
– Appliquez 20 % à 30 % de DEET ou 20 % de picaridine sur la peau exposée et suivez les instructions de réapplication du fabricant.
– Retirez les récipients d’eau ouverts autour des espaces de vie et utilisez des moustiquaires sur les fenêtres et les portes.
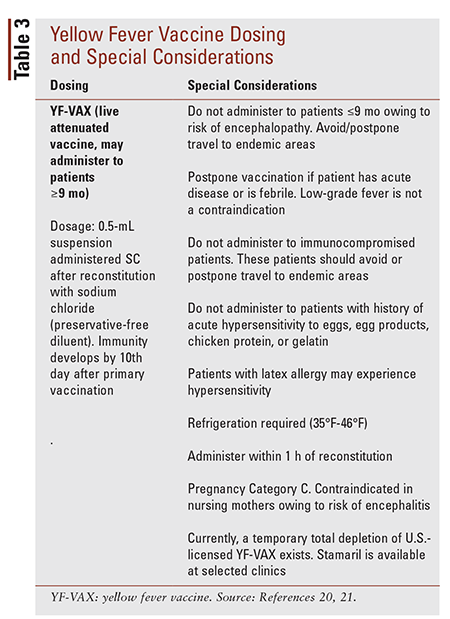
Effets indésirables : Les effets indésirables courants du YF-VAX sont les suivants : maux de tête, fièvre, gonflement et douleur au point d’injection, et douleurs ou gêne musculaires. Les effets indésirables graves sont rares, mais YF-VAX a été associé à une défaillance de plusieurs organes et à une inflammation cérébrale.20
Disponibilité : Il existe actuellement une pénurie nationale d’YV-VAX. Sanofi Pasteur, le fabricant d’YV-VAX, connaît des retards de production dus à la transition vers une nouvelle installation. La FDA a accepté une demande d’accès élargi à un nouveau médicament de recherche pour permettre l’importation de Stamaril, un vaccin produit en France par Sanofi Pasteur, pour une utilisation dans l’intervalle. Stamaril, qui est utilisé dans plus de 70 pays, est fabriqué avec la même sous-souche vaccinale que YV-VAX et est actuellement alloué pour être utilisé dans certaines cliniques aux États-Unis.22
Polio
Overview : La polio (poliomyélite) est une maladie virale infectieuse qui affecte le système nerveux central et peut provoquer une paralysie temporaire ou permanente. La polio est causée par les poliovirus de types 1, 2 et 3. Le poliovirus se transmet par contact de personne à personne ; une personne peut être infectée par de l’eau ou des aliments contaminés, par exemple, et transmettre ensuite le virus à d’autres personnes par la toux et les éternuements. Les personnes infectées sont contagieuses avant l’apparition des symptômes et jusqu’à deux semaines après leur disparition. Le poliovirus peut vivre dans les matières fécales pendant plusieurs semaines, ce qui permet au virus de se transmettre facilement dans les régions où l’assainissement est insuffisant.23 La polio est présente en Afghanistan, au Nigeria et au Pakistan, et la transmission du poliovirus dans ces pays n’a jamais été interrompue. Quatre régions sont exemptes de polio : les Amériques, l’Europe, l’Asie du Sud-Est et le Pacifique occidental.24
Symptômes : La plupart des personnes infectées par le poliovirus sont asymptomatiques. Des symptômes mineurs, notamment des maux de gorge, des maux de tête, de la fièvre, de la fatigue, des nausées et des douleurs d’estomac, apparaissent dans environ 4 à 8 % des infections. Quelques jours après la disparition des symptômes mineurs, environ 1 à 5 % des patients développent une méningite aseptique. Les symptômes graves comprennent la paralysie, la paresthésie, des problèmes cérébraux ou spinaux et une invalidité permanente ou la mort. La poliomyélite paralytique survient dans une infection sur 1 000.23,25
Diagnostic : Le prélèvement de deux échantillons de selles à 24 heures d’intervalle augmente la probabilité d’isoler le poliovirus. La méthode la plus sensible pour diagnostiquer une infection par le poliovirus consiste à isoler le virus en culture.26
Prévention : La vaccination contre le poliovirus (IPOL) est recommandée pour les personnes qui voyagent dans des pays endémiques, les travailleurs de la santé qui s’occupent de patients atteints de poliovirus et les employés de laboratoire qui manipulent des spécimens contenant du poliovirus. Voir le TABLEAU 4 pour la posologie et les considérations particulières relatives au vaccin contre la polio.23
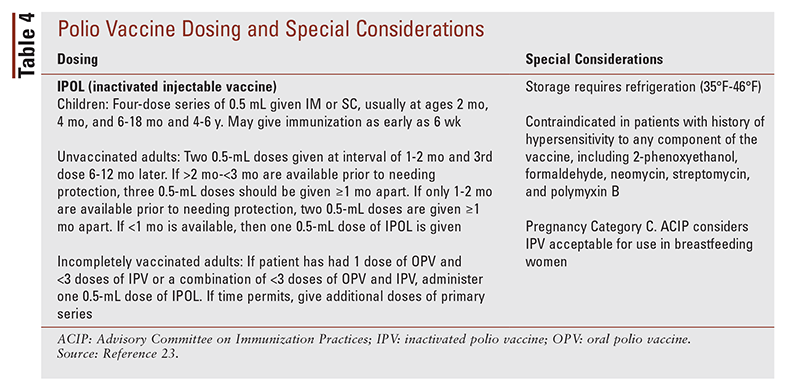
Effets indésirables : Les effets indésirables courants de l’IPOL comprennent l’enflure, la douleur au site d’injection, la fatigue, la fièvre, la perte d’appétit, les vomissements et l’irritabilité.23
Rabies
Vue d’ensemble : La salive des mammifères infectés peut transmettre le virus de la rage aux humains qui sont mordus ou griffés. Le virus de la rage peut être mortel en raison de l’encéphalomyélite. La période d’incubation peut durer de 5 jours à plusieurs années, mais elle est généralement comprise entre 20 et 60 jours. Aux États-Unis, la rage est peu fréquente chez l’homme. Les sources d’infection de la rage chez l’homme aux États-Unis comprennent les mouffettes, les renards, les ratons laveurs et les chauves-souris ; dans d’autres pays, les chiens non vaccinés en sont la cause.27
Symptômes : Les symptômes de la rage commencent par des prodromes, notamment fatigue, maux de tête, malaise, anorexie, fièvre, douleur et paresthésie. Au fur et à mesure que la maladie progresse, les patients peuvent avoir des hallucinations, des crises, de l’anxiété, de l’agitation et de l’irritabilité. Au stade avancé, les patients peuvent souffrir d’aérophobie, d’hydrophobie, d’hypersalivation, d’hyperactivité, de désorientation, de convulsions et, finalement, de paralysie, de coma et de mort27
Diagnostic : Pour confirmer que le virus de la rage a été transmis par un animal infecté à un humain, plusieurs tests sont nécessaires. Des échantillons de salive, de liquide céphalorachidien et de sérum, ainsi que des biopsies cutanées des follicules pileux de la nuque peuvent être utilisés.28
Prévention : Il existe plusieurs moyens de prévenir l’infection par la rage, notamment en évitant les animaux sauvages, en vaccinant les animaux domestiques et en consultant un médecin avant l’apparition des symptômes.29 Il est recommandé aux groupes à haut risque suivants de se faire vacciner contre la rage avant exposition, à titre préventif : spéléologues, vétérinaires et étudiants en médecine vétérinaire, manipulateurs d’animaux et personnel de laboratoire manipulant des vaccins vivants contre la rage et des immunoglobulines. En outre, la vaccination doit être envisagée pour les voyageurs internationaux qui peuvent avoir un accès limité à des soins immédiats et qui peuvent entrer en contact avec des animaux ayant la rage. Si une personne est mordue ou griffée, il est important de nettoyer la zone blessée avec de l’eau et du savon, puis d’irriguer la plaie avec un agent virucide tel que la solution de povidone iodée.30
Il existe deux formulations de vaccins antirabiques : le vaccin sur cellules diploïdes humaines (Imovax) et le vaccin purifié sur cellules d’embryon de poulet (RavAvert).31 Quatre formulations d’immunoglobulines antirabiques sont disponibles : Quatre formulations d’immunoglobulines antirabiques sont disponibles : Imogam Rabies-HT, Kedrab, HyperRAB et HyperRAB S/D.32 HyperRAB (300 UI/mL) est deux fois plus concentré que HyperRAB S/D (150 UI/mL), qui est un produit traité par solvant/détergent. Les patients recevant HyperRAB (300 UI/mL) reçoivent un volume inférieur par dose puisqu’il s’agit d’une concentration plus élevée.33
Voir le TABLEAU 5 pour la posologie et les considérations particulières relatives aux vaccins antirabiques.31,32 La vaccination pré-exposition est recommandée pour fournir une protection aux personnes présentant un risque élevé d’exposition. Elle permet également de protéger les patients qui peuvent ne pas avoir un accès immédiat aux soins en raison des délais en cas d’exposition au virus de la rage. La vaccination préexposition élimine également le besoin d’immunoglobuline, réduisant ainsi le nombre d’injections.27

Effets indésirables : Les effets indésirables courants des vaccins antirabiques comprennent une éruption au point d’injection, des douleurs abdominales, des nausées, une augmentation localisée des ganglions lymphatiques, des arthralgies, des myalgies, des vertiges, des symptômes semblables à ceux d’une flûte, des malaises et des maux de tête. Les effets indésirables graves sont l’anaphylaxie, l’encéphalite, le syndrome de Guillain-Barré et la réaction transfusionnelle due à une réaction aux protéines sériques.31
Hépatite A
Vue d’ensemble : Le virus de l’hépatite A (VHA) se transmet de personne à personne par la voie fécale-orale, par la consommation d’aliments ou d’eau contaminés. Les personnes à risque de contracter le VHA sont les voyageurs se rendant dans des pays où l’endémie est élevée ou intermédiaire, les hommes ayant des rapports sexuels avec des hommes et les utilisateurs de drogues injectables, ainsi que les personnes travaillant avec des primates non humains ; ceux qui sont en contact étroit avec une personne infectée peuvent être sensibles au virus.34,35
Diagnostic : Pour diagnostiquer le VHA, des anticorps IgG spécifiques doivent être détectés dans le sang.36
Symptômes : Les adultes présentent les symptômes suivants : fatigue, nausées, jaunisse, faible appétit et douleurs d’estomac. Les enfants âgés de moins de 6 ans ne présentent généralement pas de symptômes ou ont une infection qui n’est pas reconnue. Le VHA est généralement autolimité et n’évolue pas vers une infection chronique. Il n’existe pas de traitement pour le VHA autre que des soins de soutien tels que le repos, une alimentation équilibrée et des liquides.34
Prévention : La meilleure façon de prévenir l’infection par le VHA est la vaccination (Vaqta, Havrix), qui doit avoir lieu au moins deux semaines avant l’exposition prévue au VHA. Les anticorps produits en réponse à l’infection par le VHA confèrent une protection à vie contre la réinfection. Voir le TABLEAU 6 pour la posologie et les considérations particulières relatives aux vaccins contre l’hépatite A.35
Effets indésirables : Les effets indésirables courants des vaccins contre l’hépatite A sont la douleur, l’enflure ou l’érythème au site d’injection, la perte d’appétit, les nausées, l’irritabilité, les maux de tête, la somnolence, la fatigue, la fièvre et les malaises. Les effets indésirables graves comprennent la thrombocytopénie, la réaction anaphylactoïde, les convulsions, l’œdème de Quincke et la syncope accompagnée de signes neurologiques tels que des troubles visuels, des mouvements tonico-cloniques des membres et la paresthésie.34,35
Conclusion
Avant de voyager, il est important que les patients passent en revue les vaccins qui se rapportent à leur destination. Le site Web des CDC constitue une base de connaissances complète pour les patients et les prestataires de soins de santé. Les pharmaciens devraient conseiller les patients sur les vaccins de voyage et leurs effets indésirables, ainsi que fournir des informations sur les pratiques non pharmacologiques pour diminuer le risque de transmission.
1. CDC. La santé des voyageurs. wwwnc.cdc.gov/travel. Consulté le 15 janvier 2020.
2. CDC. Recommandations de l’ACIP. www.cdc.gov/vaccines/acip/recommendations.html. Consulté le 15 janvier 2020.
3. FDA. Ixiaro. www.fda.gov/vaccines-blood-biologics/vaccines/ixiaro. Consulté le 15 janvier 2020.
4. Organisation mondiale de la santé. Encéphalite japonaise. www.who.int/news-room/fact-sheets/detail/japanese-encephalitis. Consulté le 15 janvier 2020.
5. Hills SL, Lindsey NP, Fischer M. Encéphalite japonaise. Livre jaune 2020. wwwnc.cdc.gov/travel/yellowbook/2020/travel-related-infectious-diseases/japanese-encephalitis. Consulté le 15 janvier 2020.
6. Notice d’emballage d’Ixiaro (vaccin contre l’encéphalite japonaise). Gaithersburg, MD : Valneva USA, Inc ; septembre 2018.
7. CDC. Fièvre typhoïde et fièvre paratyphoïde. www.cdc.gov/typhoid-fever/index.html. Consulté le 15 janvier 2020.
8. Vaccines.gov. La fièvre typhoïde. www.vaccines.gov/diseases/typhoid_fever. Consulté le 15 janvier 2020.
9. CDC. Fièvre typhoïde et fièvre paratyphoïde : questions et réponses. www.cdc.gov/typhoid-fever/sources.html. Consulté le 15 janvier 2020.
10. Clinique Mayo. La fièvre typhoïde. www.mayoclinic.org/diseases-conditions/typhoid-fever/diagnosis-treatment/drc-20378665. Consulté le 15 janvier 2020.
11. CDC. Fièvre typhoïde et fièvre paratyphoïde : symptômes et traitement. www.cdc.gov/typhoid-fever/symptoms.html. Consulté le 15 janvier 2020.
12. CDC. Bulletins d’information sur le vaccin contre la typhoïde. www.cdc.gov/vaccines/hcp/vis/vis-statements/typhoid.html. Consulté le 15 janvier 2020.
13. Typhim Vi (vaccin polysaccharidique contre la typhoïde Vi) notice d’emballage. Swiftwater, PA : Sanofi Pasteur, Inc ; mars 2014.
14. Vivotif (vaccin typhoïde vivant oral Ty21a) notice d’emballage. Miami Lakes, FL : Crucell Vaccines Inc ; septembre 2013.
15. Association internationale pour l’assistance médicale aux voyageurs. La fièvre jaune. www.iamat.org/risks/yellow-fever. Consulté le 15 janvier 2020.
16. CDC. Transmission du virus de la fièvre jaune. www.cdc.gov/yellowfever/transmission/index.html. Consulté le 15 janvier 2020.
17. CDC. Vaccin contre la fièvre jaune. www.cdc.gov/yellowfever/vaccine. Consulté le 15 janvier 2020.
18. CDC. Fièvre jaune : tests de diagnostic. www.cdc.gov/yellowfever/healthcareproviders/healthcareproviders-diagnostic.html. Consulté le 15 janvier 2020.
19. Staples JE, Bocchini JA Jr, Rubin L, Fischer M. Doses de rappel du vaccin contre la fièvre jaune : recommandations du Comité consultatif sur les pratiques de vaccination, 2015. MMWR Morb Mortal Wkly Rep. 2015;64(23);647-650.
20. Notice d’accompagnement du vaccin YF-VAX (vaccin contre la fièvre jaune). Swiftwater, PA : Sanofi Pasteur, Inc ; mai 2013.
21. CDC. Annonce de mise à jour clinique : épuisement total temporaire du vaccin homologué contre la fièvre jaune aux États-Unis abordé par la disponibilité du vaccin Stamaril dans certaines cliniques. wwwnc.cdc.gov/travel/news-announcements/yellow-fever-vaccine-access. Consulté le 15 janvier 2020.
22. Sanofi. Informations sur le vaccin contre la fièvre jaune. www.sanofi.us/en/products-and-resources/vaccines/yellow-fever-vaccine-information. Consulté le 15 janvier 2020.
23. IPOL (vaccin contre le poliovirus inactivé) notice d’emballage. Swiftwater, PA : Sanofi Pasteur, Inc ; août 2015.
24. CDC. Nos progrès contre la polio. www.cdc.gov/polio/progress/index.htm. Consulté le 15 janvier 2020.
25. Passeport Santé. Qu’est-ce que la polio ? www.passporthealthusa.com/vaccinations/polio. Consulté le 15 janvier 2020.
26. CDC. Polio : méthodes de diagnostic. www.cdc.gov/polio/what-is-polio/lab-testing/diagnostic.html. Consulté le 15 janvier 2020.
27. RavAvert (vaccin contre la rage) notice d’utilisation. Research Triangle Park, NC : GlaxoSmithKline ; septembre 2019.
28. CDC. Rage : diagnostic chez l’animal et l’homme. www.cdc.gov/rabies/diagnosis/animals-humans.html. Consulté le 15 janvier 2020.
29. CDC. Vaccine information statements : rabies VIS. www.cdc.gov/vaccines/hcp/vis/vis-statements/rabies.html. Consulté le 15 janvier 2020.
30. Imovax (vaccin contre la rage) notice d’utilisation. www.vaccineshoppe.com/image.cfm?doc_id=5983&image_type=produit_pdf. Consulté le 15 janvier 2020.
31. Micromedex. Résumé du médicament pour le vaccin contre la rage. Greenwood Village, CO : Truven Health Analytics ; 2020. www.micromedexsolutions.com. Consulté le 15 janvier 2020.
32. Micromedex. Résumé du médicament pour l’immunoglobuline antirabique. Greenwood Village, CO : Truven Health Analytics ; 2020. www.micromedexsolutions.com. Consulté le 15 janvier 2020.
33. Hypermunes. HyperRAB : questions fréquemment posées. www.hypermunes.com/en/hcp/faq. Consulté le 15 janvier 2020.|
34. Organisation mondiale de la santé. Hépatite A : faits essentiels. www.who.int/news-room/fact-sheets/detail/hepatitis-a. Consulté le 15 janvier 2020.
35. CDC. Questions et réponses sur l’hépatite A pour les professionnels de la santé. www.cdc.gov/hepatitis/hav/havfaq.htm#travel. Consulté le 14 février 2020.
36. Havrix (vaccin contre l’hépatite A) notice d’emballage. Research Triangle Park, NC : GlaxoSmithKline ; décembre 2018.
37. Vaqta (vaccin contre l’hépatite A) notice d’emballage. Whitehouse Station, NJ : Merck & Co, Inc ; novembre 2019.
.