Lernziel
1. Identifizieren Sie die funktionellen Gruppen Aldehyd, Keton, Säure, Ester und Ether.
2. Verwenden Sie die korrekten Namenskonventionen für Aldehyd-, Keton-, Carbonsäure-, Ester- und Ether-haltige Moleküle.
Es gibt weitere funktionelle Gruppen, die Sauerstoffatome enthalten. Eine Carbonylgruppe wird gebildet, wenn ein O-Atom und ein C-Atom durch eine Doppelbindung verbunden sind. In diesem Diagramm stellt die R-Gruppe eine beliebige Kohlenwasserstoffkette dar:

Wenn eine Bindung der Carbonylgruppe zu einem Wasserstoffatom hergestellt wird, dann wird das Molekül weiter als Aldehyd klassifiziert. Bei der Benennung von Aldehyden muss die Hauptkette der C-Atome das Kohlenstoffatom der Carbonylgruppe einschließen, das als Position 1 in der Kohlenstoffkette nummeriert ist. Der Stammname des Kohlenwasserstoffs wird verwendet, aber das Suffix -al wird angehängt. (Verwechseln Sie -al nicht mit -ol, dem Suffix, das für Alkohole verwendet wird.) Wir haben also

Methanal hat einen gebräuchlichen Namen, den Sie vielleicht kennen: Formaldehyd. Das Wichtigste an Aldehyden ist, dass sich die Carbonylgruppe am Ende einer Kohlenstoffkette befindet.
Eine Carbonylgruppe in der Mitte einer Kohlenstoffkette bedeutet, dass die beiden verbleibenden Bindungen der Carbonylgruppe an C-Atome erfolgen. Diese Art von Molekül wird als Keton bezeichnet. Trotz der Tatsache, dass Aldehyde und Ketone die gleiche Carbonylgruppe haben, haben sie unterschiedliche chemische und physikalische Eigenschaften und werden daher richtigerweise als zwei verschiedene Arten von Verbindungen gruppiert. Das kleinste Keton hat drei C-Atome. Wenn wir ein Keton benennen, nehmen wir den Namen des übergeordneten Kohlenwasserstoffs und ändern die Endung in -one:

Der gebräuchliche Name für Propanon ist Aceton. Bei größeren Ketonen müssen wir, wie bei den Alkenen und Alkinen, eine Lokantnummer verwenden, um die Position der Carbonylgruppe kurz vor dem Suffix anzugeben:

Es gibt auch eine nicht-IUPAC-konforme Art, Ketone zu benennen: Benennen Sie die Alkylgruppen, die an die Carbonylgruppe gebunden sind, und fügen Sie das Wort Keton an den Namen an. So kann Propanon auch Dimethylketon genannt werden, während Butan-2-on Methylethylketon genannt wird.
Beispiel 9
Zeichnen Sie die Struktur von Pentan-2-on.
Lösung
Dieses Molekül hat fünf C-Atome in einer Kette, wobei die Carbonylgruppe am zweiten C-Atom sitzt. Seine Struktur ist:

Test Yourself
Zeichne die Struktur von Methylbutylketon.
Antwort

Die Kombination aus einer funktionellen Carbonylgruppe und einer Hydroxylgruppe ergibt die Carboxylgruppe.

Moleküle mit einer Carboxylgruppe werden Carbonsäuren genannt. Wie bei Aldehyden befindet sich die funktionelle Gruppe in Carbonsäuren am Ende einer Kohlenstoffkette. Ebenfalls wie bei Aldehyden wird das C-Atom in der funktionellen Gruppe als eines der C-Atome gezählt, die den Namen des übergeordneten Kohlenwasserstoffs definieren. Um Carbonsäuren zu benennen, wird der übergeordnete Name des Kohlenwasserstoffs verwendet, aber das Suffix -oic acid hinzugefügt:

Methansäure und Ethansäure werden auch Ameisensäure bzw. Essigsäure genannt. Ameisensäure ist die Verbindung, die bestimmte Ameisenbisse stechen lässt, während Essigsäure der Wirkstoff in Essig ist.
Wie sauer sind Carbonsäuren? Es stellt sich heraus, dass sie nicht sehr sauer sind. Keine Carbonsäure steht in der Liste der starken Säuren (Tabelle 12.2 „Starke Säuren und Basen“). (Weitere Informationen über starke Säuren finden Sie in Abschnitt 12.4 „Starke und schwache Säuren und Basen und ihre Salze“). Dies bedeutet, dass alle Carbonsäuren schwache Säuren sind. Eine 1 M Lösung von Ameisensäure ist nur zu etwa 1,3 % in H+-Ionen und Formiat-Ionen dissoziiert, während eine ähnliche Lösung von Essigsäure nur zu etwa 0,4 % ionisiert ist. Einige Carbonsäuren sind stärker – zum Beispiel ist Trichloressigsäure in wässriger Lösung zu etwa 45 % dissoziiert. Aber keine Carbonsäure kommt an die 100%ige Dissoziation heran, die für die Definition einer starken Säure erforderlich ist.
Wie ihr Name schon sagt, verhalten sich Carbonsäuren in Gegenwart von Basen jedoch wie Säuren. Das H-Atom in der Carboxylgruppe spaltet sich als H+-Ion ab, wobei ein Carboxylat-Ion zurückbleibt:

Carboxylat-Ionen werden nach dem Namen der Säure benannt: die -oic acid wird durch -oate ersetzt, um das Ion zu benennen.
Beispiel 10
Vervollständigen Sie die chemische Reaktion. Können Sie das gebildete Carboxylat-Ion benennen?

Lösung
Das OH- Ion entfernt das H-Atom, das Teil der Carboxylgruppe ist:

Das Carboxylat-Ion, das die kondensierte Strukturformel CH3CO2- hat, ist das Ethanoat-Ion, wird aber umgangssprachlich auch als Acetat-Ion bezeichnet.
Testen Sie sich selbst
Vervollständigen Sie die chemische Reaktion. Können Sie das gebildete Carboxylat-Ion benennen?

Antwort

Bei dem Ion handelt es sich um das Methanoat-Ion, das allgemein als Formiat-Ion bezeichnet wird.
Eine zu betrachtende Reaktion ist die von einer Carbonsäure und einem Alkohol. Wenn sie unter den richtigen Bedingungen kombiniert werden, wird ein Wassermolekül entfernt und die verbleibenden Teile verbinden sich, um eine neue funktionelle Gruppe zu bilden – die Estergruppe:

Beachten Sie, dass das Säuremolekül eine Alkylseite beiträgt (dargestellt durch R), während der Alkohol die andere Seite beiträgt (dargestellt durch R′). Ester werden mit dem Alkylgruppennamen des Alkohols und dem Carboxylatnamen der Säure benannt – dieses Molekül heißt beispielsweise Methylpropanoat.
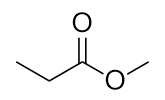
Chemie ist überall: Ester, Duft- und Aromastoffe
Ester sind sehr interessante Verbindungen, auch weil viele einen angenehmen Geruch und Geschmack haben. (Denken Sie daran, im Chemielabor nie etwas zu probieren!) Viele Ester kommen natürlich vor und tragen zum Duft von Blumen und zum Geschmack von Früchten bei. Andere Ester werden industriell synthetisiert und werden Lebensmitteln zugesetzt, um deren Geruch oder Geschmack zu verbessern. Wenn Sie ein Produkt verzehren, dessen Zutaten künstliche Aromen enthalten, ist es wahrscheinlich, dass diese Aromen Ester sind. Hier sind einige Ester und ihre Verwendungszwecke, dank ihrer Geruchs- oder Geschmacksstoffe oder beides:
| Ester | Schmeckt/Geruch wie | Ester | Schmeckt/Geruch | |
|---|---|---|---|---|
| Allyl hexanoat | Ananas | Isobutylformiat | Himbeere | |
| Benzyl Acetat | Birne | Isobutylacetat | Birne | |
| Butylbutanoat | Ananas | Methyl Phenylacetat | Honig | |
| Ethylbutanoat | Banane | Nonylcaprylat | Orange | |
| Ethylhexanoat | Ananas | Pentylacetat | Apfel | |
| Ethyl Heptanoat | Aprikose | Propylethanoat | Birne | |
| Ethylpentanoat | Apfel | Propylisobutyrat | Rum |
Schließlich, ist die funktionelle Gruppe Ether ein O-Atom, das an zwei organische Gruppen gebunden ist:
R-O-R′
Die beiden R-Gruppen können gleich oder verschieden sein. Die Benennung von Ethern entspricht der alternativen Benennung von Ketonen. In diesem Fall werden die R-Gruppen nacheinander benannt und das Wort Ether angehängt. Das Molekül CH3OCH3 ist Dimethylether, während CH3OCH2CH3 Methylethylether ist. Diethylether, ein weiterer Ether, wurde früher als Anästhetikum verwendet, aber seine Entflammbarkeit und Toxizität ließen ihn in Ungnade fallen. Kleinere Ethermoleküle, die bei Raumtemperatur flüssig sind, sind gängige Lösungsmittel für organisch-chemische Reaktionen.
Key Takeaways
- Aldehyde, Ketone, Carbonsäuren, Ester und Ether haben sauerstoffhaltige funktionelle Gruppen.
- IUPAC-Namen können für aldehyd-, keton-, carbonsäure-, ester- und etherhaltige Moleküle verwendet werden.
Übungen
-
Nennen Sie eine Ähnlichkeit zwischen den funktionellen Gruppen, die in Aldehyden und Ketonen vorkommen. Können Sie einen Unterschied zwischen ihnen nennen?
-
Erläutern Sie, wie aus einer Carbonsäure ein Ester entsteht.
-
Benennen Sie jedes Molekül.
a)
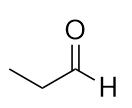
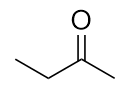
b)
-
Benennen Sie jedes Molekül.
a)
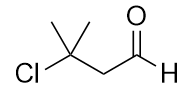
b)
-
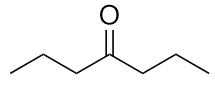
Benennen Sie jedes Molekül.
a)
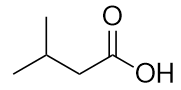
b)
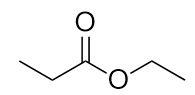
-
Benennen Sie jedes Molekül.
a)
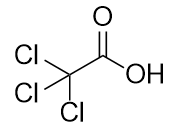
b)
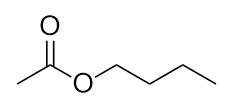
-
Nennen Sie dieses Molekül.
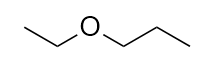
-
Benennen Sie dieses Molekül.
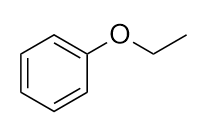
-
Nennen Sie einen alternativen, aber akzeptablen Namen für das Molekül aus Übung 3.2.
-
Geben Sie einen alternativen, aber akzeptablen Namen für das Molekül in Übung 4.2 an.
-
Vervollständigen Sie diese chemische Reaktion.
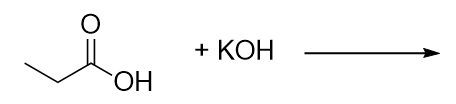
-
Vervollständigen Sie diese chemische Reaktion.
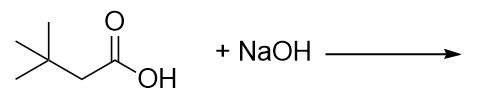
-
Das Medikament Aspirin hat diese Molekülstruktur:
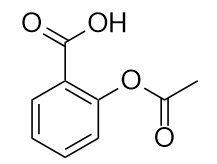
Ermitteln Sie die funktionelle(n) Gruppe(n) in diesem Molekül.
-
Das als Naproxen-Natrium bekannte Medikament ist das Natriumsalz dieses Moleküls:
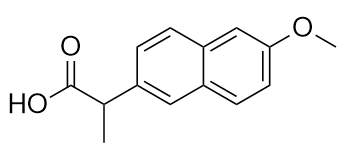
Bestimmen Sie die funktionelle(n) Gruppe(n) in diesem Molekül.
-
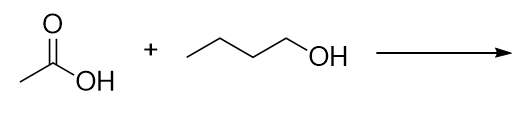
Identifizieren Sie den Ester, der durch die Reaktion dieser Moleküle entsteht.
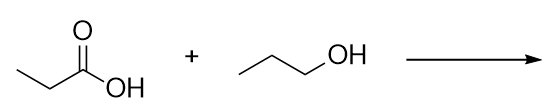
-
Identifizieren Sie den Ester, der durch die Reaktion dieser Moleküle entsteht.
Antworten
1. Beide haben eine Carbonylgruppe, aber bei einem Aldehyd befindet sich die Carbonylgruppe am Ende einer Kohlenstoffkette, und bei einem Keton ist das Carbonylkohlenstoff von zwei anderen Kohlenstoffen umgeben.
a) Propanal
b) Butan-2-ein
a) 3-Methylbutansäure
b) Ethylpropionat
7. Ethylpropylether
9. Ethylmethylketon
11. H2O + KCH3CH2CO213. Säure, Ester, und aromatisch (Benzolring)
15. Propylpropionat