DNA-SchädenBearbeiten

DNA-Schäden gelten als Hauptursache für bösartige Neoplasmen, die als Krebs bekannt sind. Ihre zentrale Rolle bei der Entstehung von Krebs ist in der Abbildung in diesem Abschnitt im Kasten oben dargestellt (die zentralen Merkmale von DNA-Schäden, epigenetischen Veränderungen und mangelhafter DNA-Reparatur bei der Entstehung von Krebs sind in rot dargestellt). DNA-Schäden sind sehr häufig. Natürlich auftretende DNA-Schäden (hauptsächlich durch den Zellstoffwechsel und die Eigenschaften der DNA in Wasser bei Körpertemperatur) treten mit einer Rate von durchschnittlich mehr als 60.000 neuen Schäden pro menschlicher Zelle pro Tag auf. Zusätzliche DNA-Schäden können durch die Exposition gegenüber exogenen Substanzen entstehen. Tabakrauch verursacht erhöhte exogene DNA-Schäden, und diese DNA-Schäden sind die wahrscheinliche Ursache für Lungenkrebs durch Rauchen. UV-Licht aus der Sonnenstrahlung verursacht DNA-Schäden, die beim Melanom eine Rolle spielen. Eine Helicobacter pylori-Infektion produziert hohe Mengen an reaktiven Sauerstoffspezies, die die DNA schädigen und zur Entstehung von Magenkrebs beitragen. Gallensäuren, die in hohen Konzentrationen in den Dickdärmen von Menschen mit fettreicher Ernährung vorkommen, verursachen ebenfalls DNA-Schäden und tragen zu Dickdarmkrebs bei. Katsurano et al. wiesen darauf hin, dass Makrophagen und Neutrophile in einem entzündeten Kolonepithel die Quelle reaktiver Sauerstoffspezies sind, die die DNA-Schäden verursachen, die die Kolontumorigenese einleiten. Einige Quellen von DNA-Schäden sind in den Kästen am oberen Rand der Abbildung in diesem Abschnitt angegeben.
Individuen mit einer Keimbahnmutation, die einen Mangel in einem von 34 DNA-Reparaturgenen verursacht (siehe Artikel DNA-Reparatur-Mangelerkrankung), haben ein erhöhtes Krebsrisiko. Einige Keimbahnmutationen in DNA-Reparaturgenen verursachen ein bis zu 100%iges Lebenszeitrisiko für Krebs (z.B. p53-Mutationen). Diese Keimbahnmutationen sind in einem Kasten links in der Abbildung mit einem Pfeil gekennzeichnet, der ihren Beitrag zur DNA-Reparaturstörung anzeigt.
Ungefähr 70% der bösartigen Neubildungen haben keine erbliche Komponente und werden als „sporadische Krebserkrankungen“ bezeichnet. Nur eine Minderheit der sporadischen Krebserkrankungen hat einen Mangel in der DNA-Reparatur aufgrund einer Mutation in einem DNA-Reparatur-Gen. Die Mehrheit der sporadischen Krebserkrankungen weist jedoch einen Mangel an DNA-Reparatur auf, der auf epigenetische Veränderungen zurückzuführen ist, die die Expression von DNA-Reparaturgenen reduzieren oder ausschalten. Zum Beispiel hatten von 113 sequenziellen kolorektalen Karzinomen nur vier eine Missense-Mutation im DNA-Reparatur-Gen MGMT, während die Mehrheit eine reduzierte MGMT-Expression aufgrund einer Methylierung der MGMT-Promotorregion (eine epigenetische Veränderung) aufwies. In fünf Berichten wurde nachgewiesen, dass zwischen 40 und 90 % der kolorektalen Karzinome eine reduzierte MGMT-Expression aufgrund von Methylierung der MGMT-Promotorregion aufweisen.
In ähnlicher Weise war von 119 Fällen von Mismatch-Reparatur-defizienten kolorektalen Karzinomen, denen die Expression des DNA-Reparatur-Gens PMS2 fehlte, PMS2 in 6 Fällen aufgrund von Mutationen im PMS2-Gen defizitär, während in 103 Fällen die PMS2-Expression defizitär war, weil sein Paarungspartner MLH1 aufgrund von Promotor-Methylierung unterdrückt war (das PMS2-Protein ist in Abwesenheit von MLH1 instabil). In den anderen 10 Fällen war der Verlust der PMS2-Expression wahrscheinlich auf eine epigenetische Überexpression der microRNA miR-155 zurückzuführen, die MLH1 herunterreguliert.
In weiteren Beispielen wurden epigenetische Defekte in Häufigkeiten zwischen 13%-100% für die DNA-Reparaturgene BRCA1, WRN, FANCB, FANCF, MGMT, MLH1, MSH2, MSH4, ERCC1, XPF, NEIL1 und ATM gefunden. Diese epigenetischen Defekte traten bei verschiedenen Krebsarten auf (z. B. Brust-, Eierstock-, Darm- und Kopf-Hals-Krebs). Zwei oder drei Defizite in der Expression von ERCC1, XPF oder PMS2 treten gleichzeitig in der Mehrzahl der 49 von Facista et al. untersuchten Dickdarmkarzinome auf. Epigenetische Veränderungen, die zu einer reduzierten Expression von DNA-Reparaturgenen führen, werden in diesem Abschnitt in einem zentralen Kasten auf der dritten Ebene von oben dargestellt, und der daraus resultierende DNA-Reparaturdefekt wird auf der vierten Ebene gezeigt.
Wenn die Expression von DNA-Reparaturgenen reduziert ist, akkumulieren DNA-Schäden in den Zellen auf einem höheren als dem normalen Niveau, und diese überschüssigen Schäden verursachen erhöhte Mutations- oder Epimutationshäufigkeiten. Die Mutationsraten steigen in Zellen, die in der DNA-Mismatch-Reparatur oder in der homologen rekombinativen Reparatur (HRR) defekt sind, stark an.
Bei der Reparatur von DNA-Doppelstrangbrüchen oder der Reparatur anderer DNA-Schäden können unvollständig geräumte Reparaturstellen epigenetisches Gen-Silencing verursachen. DNA-Reparaturdefekte (Ebene 4 in der Abbildung) verursachen vermehrte DNA-Schäden (Ebene 5 in der Abbildung), die zu vermehrten somatischen Mutationen und epigenetischen Veränderungen (Ebene 6 in der Abbildung) führen.
Felddefekte, normal erscheinendes Gewebe mit multiplen Veränderungen (und im folgenden Abschnitt besprochen), sind häufige Vorläufer für die Entwicklung des gestörten und unangemessen proliferierenden Gewebeklons in einem malignen Neoplasma. Solche Felddefekte (zweite Ebene von unten in der Abbildung) können multiple Mutationen und epigenetische Veränderungen aufweisen.
Wenn sich ein Krebs gebildet hat, weist er in der Regel eine Instabilität des Genoms auf. Diese Instabilität ist wahrscheinlich auf eine reduzierte DNA-Reparatur oder übermäßige DNA-Schäden zurückzuführen. Aufgrund einer solchen Instabilität entwickelt sich der Krebs weiter und produziert Subklone. Zum Beispiel hatte ein Nierenkrebs, der in 9 Bereichen beprobt wurde, 40 ubiquitäre Mutationen, die Tumorheterogenität demonstrieren (d.h. in allen Bereichen des Krebses vorhanden), 59 Mutationen, die von einigen (aber nicht allen Bereichen) geteilt werden, und 29 „private“ Mutationen, die nur in einem der Bereiche des Krebses vorhanden sind.
FelddefekteBearbeiten
Verschiedene andere Begriffe wurden verwendet, um dieses Phänomen zu beschreiben, einschließlich „Feldeffekt“, „Feldkanzerisierung“ und „Feldkarzinogenese“. Der Begriff „Feldkanzerisierung“ wurde erstmals 1953 verwendet, um einen Bereich oder ein „Feld“ des Epithels zu beschreiben, das durch (damals noch) weitgehend unbekannte Prozesse so präkonditioniert wurde, dass es für die Entwicklung von Krebs prädisponiert ist. Seitdem werden die Begriffe „Feldkanzerisierung“ und „Felddefekt“ verwendet, um prämalignes Gewebe zu beschreiben, in dem wahrscheinlich neue Krebsarten entstehen.
Felddefekte sind wichtig für die Progression zu Krebs. Doch in den meisten Krebsforschungen, wie Rubin betont, „wurde die überwiegende Mehrheit der Studien in der Krebsforschung an gut definierten Tumoren in vivo oder an diskreten neoplastischen Foci in vitro durchgeführt. Es gibt jedoch Hinweise darauf, dass mehr als 80 % der somatischen Mutationen, die in menschlichen kolorektalen Tumoren mit Mutator-Phänotyp gefunden werden, vor dem Beginn der terminalen klonalen Expansion auftreten. In ähnlicher Weise weisen Vogelstein et al. darauf hin, dass mehr als die Hälfte der in Tumoren identifizierten somatischen Mutationen in einer prä-neoplastischen Phase (in einem Felddefekt), während des Wachstums scheinbar normaler Zellen, auftraten. Ebenso können epigenetische Veränderungen, die in Tumoren vorhanden sind, in prä-neoplastischen Felddefekten entstanden sein.
Eine erweiterte Sichtweise des Feldeffekts wird als „ätiologischer Feldeffekt“ bezeichnet, der nicht nur molekulare und pathologische Veränderungen in prä-neoplastischen Zellen, sondern auch Einflüsse exogener Umweltfaktoren und molekulare Veränderungen in der lokalen Mikroumgebung auf die neoplastische Entwicklung von der Tumorinitiation bis zum Tod des Patienten umfasst.
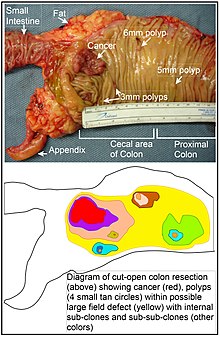
Im Dickdarm entsteht ein Felddefekt wahrscheinlich durch natürliche Selektion einer mutierten oder epigenetisch veränderten Zelle unter den Stammzellen an der Basis einer der Darmkrypten an der Innenseite des Dickdarms. Eine mutierte oder epigenetisch veränderte Stammzelle kann durch natürliche Selektion die anderen Stammzellen in der Nähe ersetzen. So kann ein Fleck mit abnormalem Gewebe entstehen. Die Abbildung in diesem Abschnitt enthält ein Foto eines frisch resezierten und der Länge nach aufgeschnittenen Dickdarmsegments, das einen Dickdarmkrebs und vier Polypen zeigt. Unter dem Foto befindet sich ein schematisches Diagramm, das zeigt, wie sich ein großer Fleck mutierter oder epigenetisch veränderter Zellen gebildet haben könnte, dargestellt durch den großen gelben Bereich im Diagramm. Innerhalb dieses ersten großen Flecks im Diagramm (ein großer Klon von Zellen) kann eine zweite solche Mutation oder epigenetische Veränderung auftreten, so dass eine bestimmte Stammzelle einen Vorteil im Vergleich zu anderen Stammzellen innerhalb des Flecks erhält, und diese veränderte Stammzelle kann sich klonal ausbreiten und einen zweiten Fleck oder Subklon innerhalb des ursprünglichen Flecks bilden. Dies wird im Diagramm durch vier kleinere Flecken mit unterschiedlichen Farben innerhalb des großen gelben Originalbereichs angezeigt. Innerhalb dieser neuen Flecken (Subklone) kann sich der Prozess mehrfach wiederholen, angezeigt durch die noch kleineren Flecken innerhalb der vier sekundären Flecken (mit immer noch unterschiedlichen Farben im Diagramm), die sich klonal ausdehnen, bis Stammzellen entstehen, die entweder kleine Polypen oder aber ein bösartiges Neoplasma (Krebs) erzeugen.
Im Bild hat ein offensichtlicher Felddefekt in diesem Segment eines Dickdarms vier Polypen erzeugt (beschriftet mit der Größe der Polypen, 6 mm, 5 mm und zwei von 3 mm, sowie ein Krebsgeschwür von etwa 3 cm Durchmesser in seiner längsten Ausdehnung). Diese Neoplasmen werden auch in dem Diagramm unter dem Foto durch 4 kleine hellbraune Kreise (Polypen) und einen größeren roten Bereich (Krebs) angezeigt. Der Krebs auf dem Foto ist im zökalen Bereich des Dickdarms aufgetreten, dort, wo der Dickdarm in den Dünndarm übergeht (beschriftet) und wo der Blinddarm liegt (beschriftet). Das Fett auf dem Foto befindet sich außen an der Außenwand des Dickdarms. Bei dem hier gezeigten Dickdarmsegment wurde der Dickdarm der Länge nach aufgeschnitten, um die innere Oberfläche des Dickdarms freizulegen und den Krebs und die Polypen zu zeigen, die in der inneren Epithelauskleidung des Dickdarms auftreten.
Wenn der allgemeine Prozess, durch den sporadische Kolonkarzinome entstehen, die Bildung eines prä-neoplastischen Klons ist, der sich durch natürliche Selektion ausbreitet, gefolgt von der Bildung interner Sub-Klone innerhalb des initialen Klons und Sub-Sub-Klonen innerhalb dieser, dann sollten Kolonkarzinome im Allgemeinen mit Bereichen zunehmender Abnormalität assoziiert sein und diesen vorausgehen, die die Abfolge prämaligner Ereignisse widerspiegeln. Die ausgedehnteste Region der Abnormalität (der äußerste gelbe unregelmäßige Bereich im Diagramm) würde das früheste Ereignis bei der Bildung eines bösartigen Neoplasmas widerspiegeln.
Bei der experimentellen Auswertung spezifischer DNA-Reparaturdefekte in Krebserkrankungen wurde gezeigt, dass viele spezifische DNA-Reparaturdefekte auch in den Felddefekten auftreten, die diese Krebserkrankungen umgeben. In der folgenden Tabelle sind Beispiele aufgeführt, bei denen gezeigt wurde, dass der DNA-Reparaturmangel in einem Krebs durch eine epigenetische Veränderung verursacht wurde, und die etwas geringeren Häufigkeiten, mit denen derselbe epigenetisch verursachte DNA-Reparaturmangel in dem umgebenden Felddefekt gefunden wurde.
| Krebs | Gen | Häufigkeit bei Krebs | Häufigkeit bei Felddefekt | Ref. |
|---|---|---|---|---|
| Kolorektal | MGMT | 46% | 34% | |
| Kolorektal | MGMT | 47% | 11% | |
| Kolorektal | MGMT | 70% | 60% | |
| Kolorektal | MSH2 | 13% | 5% | |
| Kolorektal | ERCC1 | 100% | 40% | |
| Kolorektal | PMS2 | 88% | 50% | |
| Kolorektal | XPF | 55% | 40% | |
| Kopf und Hals | MGMT | 54% | 38% | |
| Kopf und Hals | MLH1 | 33% | 25% | |
| Kopf und Hals | MLH1 | 31% | 20% | |
| Magen | MGMT | 88% | 78% | |
| Magen | MLH1 | 73% | 20% | |
| Ösophagus | MLH1 | 77%-100% | 23%-79% |
Ein Teil der kleinen Polypen im Felddefekt, die auf dem Foto des geöffneten Dickdarmsegments zu sehen sind, können relativ gutartige Neubildungen sein. Von den Polypen mit einer Größe von weniger als 10 mm, die bei der Koloskopie gefunden und durch wiederholte Koloskopien über einen Zeitraum von 3 Jahren verfolgt wurden, blieben 25 % in ihrer Größe unverändert, 35 % bildeten sich zurück oder schrumpften, während 40 % an Größe zunahmen.
Genom-InstabilitätBearbeiten
Krebs ist dafür bekannt, dass er eine Genom-Instabilität oder einen Mutator-Phänotyp aufweist. Die proteinkodierende DNA innerhalb des Zellkerns macht etwa 1,5 % der gesamten genomischen DNA aus. Innerhalb dieser proteinkodierenden DNA (Exom genannt) kann ein durchschnittlicher Brust- oder Darmkrebs etwa 60 bis 70 proteinverändernde Mutationen aufweisen, von denen etwa 3 oder 4 „Treiber“-Mutationen und die übrigen „Passagier“-Mutationen sein können. Die durchschnittliche Anzahl von DNA-Sequenzmutationen im gesamten Genom (einschließlich nicht-proteinkodierender Regionen) in einer Brustkrebs-Gewebeprobe beträgt jedoch etwa 20.000. In einer durchschnittlichen Melanom-Gewebeprobe (wobei Melanome eine höhere Exom-Mutationsfrequenz aufweisen) beträgt die Gesamtzahl der DNA-Sequenzmutationen etwa 80.000. Dies steht im Vergleich zu der sehr geringen Mutationshäufigkeit von etwa 70 neuen Mutationen im gesamten Genom zwischen den Generationen (von Eltern zu Kindern) beim Menschen.
Die hohen Häufigkeiten von Mutationen in den gesamten Nukleotidsequenzen innerhalb von Krebserkrankungen deuten darauf hin, dass oft eine frühe Veränderung in den Felddefekten, die zu einer Krebserkrankung führen (z. B. gelber Bereich in der Grafik in diesem Abschnitt), ein Mangel in der DNA-Reparatur ist. Facista et al. zeigten, dass die großen Felddefekte, die Dickdarmkrebs umgeben (die sich bis zu etwa 10 cm auf jeder Seite eines Krebses erstrecken), häufig epigenetische Defekte in 2 oder 3 DNA-Reparaturproteinen (ERCC1, XPF oder PMS2) im gesamten Bereich des Felddefekts aufweisen. Defekte in der DNA-Reparatur verursachen erhöhte Mutationsraten. Ein Mangel in der DNA-Reparatur selbst kann dazu führen, dass sich DNA-Schäden anhäufen, und die fehleranfällige Translesionssynthese an einigen dieser Schäden vorbei kann zu Mutationen führen. Darüber hinaus kann eine fehlerhafte Reparatur dieser akkumulierten DNA-Schäden zu Epimutationen führen. Diese neuen Mutationen oder Epimutationen können einen Proliferationsvorteil verschaffen und einen Felddefekt erzeugen. Obwohl die Mutationen/Epimutationen in DNA-Reparaturgenen selbst keinen Selektionsvorteil bieten, können sie als Passagiere in Zellen mitgeführt werden, wenn die Zellen zusätzliche Mutationen/Epimutationen erwerben, die einen Proliferationsvorteil bieten.