Der Einsatz von Phosphatbindern ist eines der grundlegenden Elemente in der Behandlung von CKD-MBD („Chronic Kidney Disease-Mineral and Bone Disorder“).1
Seit Jahrzehnten ist bekannt, dass die Phosphatretention durch direkte und indirekte Mechanismen zur Entstehung und Progression des sekundären Hyperparathyreoidismus (SHP) und der renalen Osteodystrophie bei chronischen Nierenerkrankungen (CKD) beiträgt.1,2 Tatsächlich blockiert die Phosphatretention alle hormonellen Gegenregulationsmechanismen, erhöht die Skelettwiderstandsfähigkeit gegenüber PTH und gilt als zentraler Faktor in der Physiopathologie anderer endokriner und systemischer Veränderungen wie der Abnahme von Calcitriol, der Zunahme des Fibroblasten-Wachstumsfaktors-23 (FGF-23), kardiovaskulären Verkalkungen, vorzeitiger Alterung und der hohen Morbidität dieser Patienten.2,3 Aus all diesen Gründen gilt Phosphat als „der stille Killer“ von Patienten mit CKD.4
Die aktuellen KDIGO-Leitlinien betonen daher insbesondere bei Dialysepatienten die Bedeutung einer diätetischen Phosphatrestriktion, einer adäquaten Dialysedosis und des Einsatzes von Phosphatbindern.2 Die Evidenz über die positive Wirkung der Diät ist begrenzt und von geringer Qualität5 und eine aggressive Phosphatrestriktion ist nicht nur schwierig, sondern könnte auch den Ernährungszustand des Patienten beeinträchtigen, was den Nutzen der Phosphorkontrolle aufwiegen würde.6 Tatsächlich würde der Einsatz von Phosphatbindern eine freizügigere Diät und ein geringeres Risiko der Mangelernährung ermöglichen.
Obwohl per Definition alle Phosphatbinder die Serumspiegel von Phosphat senken, scheinen die Eigenschaften der Phosphatbinder (mit Kalzium, ohne Kalzium, mit Metallen wie Magnesium, Eisen oder Aluminium; Polymere) in der Monotherapie oder in Kombination unterschiedliche Auswirkungen auf verschiedene Aspekte des CKD-MBD-Komplexes (z. B. arterielle Verkalkung, FGF-23-Spiegel) oder auf das Überleben von Dialysepatienten zu bedingen.7,8 Die neuen KDIGO-Leitlinien 2017 haben den Grad der Evidenz für die Notwendigkeit erhöht, die Verwendung von kalziumhaltigen Phosphatbindern bei allen CKD-Patienten einzuschränken (Evidenz 2B)2 , und diese Einschränkung gilt nicht nur für Patienten mit Hyperkalzämie, arterieller Verkalkung, adynamischer Knochenerkrankung oder Patienten mit anhaltend erniedrigtem Parathormon (PTH), wie in früheren Leitlinien vorgeschlagen. Ebenso wird es nach wie vor als sinnvoll erachtet, das Vorhandensein von vaskulären/valvulären Verkalkungen bei Patienten mit CKD zu beurteilen, um das pharmakologische Management zu steuern.2,9
Binder: Adhärenz und pharmakologische Interaktionen
Nephrologen sind sich im Allgemeinen bewusst, dass Patienten mit CKD, insbesondere unter Nierenersatztherapie, eine große Anzahl von Medikamenten einnehmen müssen und viele davon Phosphatbinder in Form von Tabletten/Kapseln/Tagesbeuteln sind.10 Die gleichzeitige Verabreichung von mehreren Medikamenten an denselben Patienten ist sehr häufig. Obwohl diese Situation vorteilhaft sein kann, um die Therapietreue zu verbessern, gibt es einige Nachteile, wie die Möglichkeit von pharmakologischen Wechselwirkungen, insbesondere bei Patienten im fortgeschrittenen Alter oder mit chronischen Erkrankungen.
Ein Aspekt, der von Nephrologen oft vergessen wird, ist, dass Phosphatbinder aufgrund ihrer unterschiedlichen biochemischen Eigenschaften einen ausgeprägten differentiellen Einfluss auf die Absorption und Wirksamkeit vieler Medikamente haben können. In der Tat ist ihre gleichzeitige Verabreichung mit anderen Medikamenten häufig und ihre möglichen klinischen Auswirkungen werden häufig nicht bemerkt. Daher halten wir es für wichtig, diese Praxis zu verbessern und die beschriebenen pharmakologischen Wechselwirkungen der verschiedenen Phosphatbinder zu überprüfen.
Pharmakologische Wechselwirkungen
Die unterschiedliche Wirkung von Phosphatbindern auf die Absorption anderer Arzneimittel impliziert eine pharmakokinetische Wechselwirkung (die im Allgemeinen die Absorption beeinflusst), die sich von pharmakodynamischen Wechselwirkungen (die die Bindung an Rezeptoren beeinflussen oder Mechanismen der Signaltransduktion verändern) unterscheidet. Es gibt viele Übersichtsarbeiten und Tabellen, die die verschiedenen Wirkungen von Phosphatbindern zusammenfassen (Dosis, Anzahl der Tabletten, Nebenwirkungen, Kalzium-, Phosphat-, PTH- und FGF-23-Spiegel und sogar auf das Fortschreiten der Gefäßverkalkung und/oder das Überleben/die Sterblichkeit)9; es gibt jedoch keine Publikationen, die mögliche Arzneimittelinteraktionen wie die in Abbildung 1 zusammengefassten analysieren und vergleichen. Es ist zu erkennen, dass die meisten Arzneimittelinteraktionen mit kalzium- und aluminiumhaltigen Phosphatbindern beobachtet werden.

Erhöht das Risiko von Hyperkalzämie und sekundärer pharmakologischer Toxizität (z. B. Digitalis). Weder Sevelamer noch Lanthan wurden in Verbindung mit Diuretika untersucht, aber Hyperkalzämie ist keine Nebenwirkung.

Keine Wechselwirkung (nachgewiesen in in vitro oder in vivo Studien).

Unspezifische Wechselwirkung.

Nicht beschrieben, aber mit einem möglichen Klasseneffekt.

Nicht beschrieben, aber mit möglicher Klassenwirkung, auch mit Furosemid und Losartan.‘ >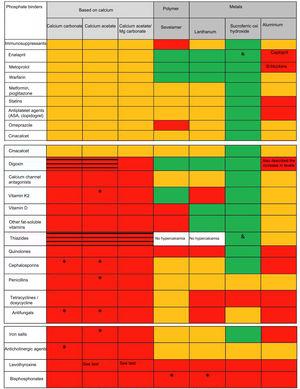
Pharmakologische Wechselwirkungen von großer nephrologischer Bedeutung der verschiedenen in Spanien erhältlichen Phosphatbinder.
# Siehe Text. Aluminiumhydroxid kann die Konzentration von Valproinsäure erhöhen (obwohl die klinische Bedeutung nicht nachgewiesen ist), und Intoxikationen wurden für Chinidin und Digoxin beschrieben. Außerdem verringert es die Absorption oder senkt die Konzentration von Allopurinol und Sucralfat, NSAIDs, Carbenoxolon, Chlorpromazin, Epoetin, Ketoconazol, Ethambutol, Gabapentin, Isoniazid, Metronidazol, Penicillamin, Ranitidin, Chloroquin, Cycline, Diflunisal, Natriumfluorid, Glukokortikoide, Kayexalat, Lincosamide, Phenothiazine und Neuroleptika, Cefpodoxim, Isoniazid und Nitrofurantoin. Erwähnenswert ist die Abnahme der Kortikosteroid-Resorption, allerdings mit zweifelhaften klinischen Auswirkungen, wenn das Ansprechen auf das Medikament überwacht wird. Es ist bekannt, dass die Toxizität durch Natriumcitrat und Vitamin C erhöht wird. Es erhöht die Ausscheidung von Acetylsalicylsäure und kann die Verteilung von Natriumpertechnetat in Radioimaging-Tests verändern.

Reduzierte Absorption/verringerte Effizienz

Erhöhtes Risiko für Hyperkalzämie und sekundäre pharmakologische Toxizität (i.e. Digitalis). Weder Sevelamer noch Lanthan wurden in Verbindung mit Diuretika untersucht, aber Hyperkalzämie ist keine Nebenwirkung.

Keine Wechselwirkung (nachgewiesen in in vitro oder in vivo Studien).

Unspezifische Wechselwirkung.

Nicht beschrieben, aber mit einem möglichen Klasseneffekt.

Das Fehlen von Wechselwirkungen wurde auch mit Furosemid und Losartan nachgewiesen.
Calcium-basierte PhosphatbinderCalciumcarbonat (Mastical®, Caosina®)
Calciumcarbonat kann die Absorption verschiedener Medikamente verändern, daher sollten diese mindestens 2h vor oder 4-6h nach dem Binder verabreicht werden. Zusätzlich zu den gezeigten Medikamenten sind andere Antibiotika wie Neomycin, Chloramphenicol und Fosfomycin, systemische Kortikosteroide, Phenytoin, Barbiturate, Antazida, die Aluminiumsalze enthalten, Cholestyramin, Zink, Fluoride und Eisensalze hervorzuheben.11,12 Diese letzte Wechselwirkung ist wichtig, um Kombinationen der häufig verwendeten Phosphatbinder auf Calciumbasis8 mit eisenhaltigen Bindemitteln zu vermeiden. Wie bei den anderen Bindemitteln beobachtet, ist es wichtig zu beachten, dass die Wirksamkeit von Levothyroxin durch die gleichzeitige Anwendung von Calciumbindern reduziert werden kann. Das bedeutet, dass die Verabreichung von Kalziumkarbonat und Levothyroxin mindestens 4 Stunden auseinander liegen sollte.13
Eine weitere zu berücksichtigende Interaktion, diese ist pharmakodynamischer Natur, besteht darin, dass eine Hyperkalzämie die Toxizität von Digitalis (Digoxin) erhöhen kann und dass Thiaziddiuretika die Kalziumausscheidung im Urin verringern, so dass bei gleichzeitiger Verabreichung von kalziumhaltigen Phosphatbindern ein erhöhtes Risiko einer Hyperkalzämie besteht. Ebenso kann die gleichzeitige Behandlung mit Vitamin-D-Derivaten und/oder calciumhaltigen Medikamenten oder Nährstoffen (Milch) eine Hypercalcämie und das Milch-Alkali-Syndrom begünstigen. Außerdem kann die Einnahme hoher Calciummengen zu einer Ausfällung von Galle und Fettsäuren in Form von Seifen führen, die die Resorption von Ursodesoxychol- und Chenodesoxycholsäure sowie von Fetten und fettlöslichen Vitaminen verändern können.12,13
Calciumacetat (Royen®, RenaCare® Calciumacetat)
Wie bei Calciumcarbonat erwähnt, kann die Verabreichung von Calciumacetat mit einigen Medikamenten dessen Resorption verändern oder deren Toxizität durch Hypercalcämie begünstigen. Zusätzlich zu den in der Tabelle dargestellten Informationen sollte der kaum bekannte Effekt auf die Beeinträchtigung der Wirksamkeit von Kalziumantagonisten hervorgehoben werden.14 Obwohl eine retrospektive pharmakoepidemiologische Studie auf die geringe oder keine Beeinträchtigung der Absorption von Levothyroxin durch Kalziumacetat hingewiesen hatte,15 legen neuere Daten nahe, dass Hypothyreose-Patienten davor gewarnt werden sollten, die Dosis von Levothyroxin deutlich getrennt von jeder Formulierung mit Kalzium einzunehmen.16
Calciumacetat/Magnesiumcarbonat (Osvaren®)
Die Kombination Calciumacetat/Magnesiumcarbonat kann die Absorption einiger in der Tabelle aufgeführter Medikamente verändern, so dass diese nicht innerhalb von 2h vor oder 3h nach der Einnahme des Phosphatbinders eingenommen werden sollten.17 Neben der Verringerung der Absorption von Cefuroxim, Cefpodoxim oder Nitrofurantoin wird auch die Wechselwirkung mit der Absorption von Zink, Fluoriden und dem Malariamittel Halofantrin beschrieben.17 Ebenso kann die Einnahme von Magnesium die Absorption von Eisen beeinflussen, einer häufigen Ergänzung in der Polymedikation des Patienten mit CKD. Calciumacetat/Magnesiumcarbonat kann ebenfalls eine Hypermagnesiämie hervorrufen, weshalb Antazida, die nicht nur Calcium- sondern auch Magnesiumsalze enthalten, vermieden werden sollten. Magnesiumsalze können die Absorption von Digoxin im Gastrointestinaltrakt begünstigen, wodurch seine Bioverfügbarkeit verringert wird, zusätzlich zu der Möglichkeit, seine potenzielle Toxizität aufgrund einer Hyperkalzämie zu erhöhen. In der Zusammenfassung der Produktmerkmale dieser Kombination wird die Möglichkeit beschrieben, dass die gleichzeitige Anwendung mit Östrogenen einen Anstieg des Serumkalziumspiegels verursachen kann.17 Interessanterweise wird im Gegensatz zu den anderen Bindemitteln erwähnt, dass es zu einer erhöhten Absorption von Levothyroxin kommen kann, wenn es in Kombination mit Aluminiumhydroxid verabreicht wird17,18; wie bereits erwähnt, deuten neuere Daten jedoch darauf hin, dass die Verabreichung von Levothyroxin klar von jeder Formulierung mit Calcium16 und anderen Bindemitteln getrennt werden sollte.
Bindemittel ohne Calcium: Polymere und Metalle
Wie in Abbildung 1 dargestellt, ist die Anzahl der beschriebenen pharmakologischen Wechselwirkungen mit Bindemitteln mit Polymerstruktur (Sevelamer) oder Metallen (Lanthan, Eisen) geringer als die von calciumbasierten Phosphatbindern. Allerdings gibt es eine Fülle von Informationen über Arzneimittelinteraktionen dieser Bindemittel, da sie erst in jüngerer Zeit in das therapeutische Arsenal aufgenommen wurden und diese Medikamente in ihren klinischen Studien mehr Anfragen an die offiziellen Stellen richten mussten. Wir betonen, dass in diesen Studien Patienten, die Antiarrhythmika oder Antikonvulsiva einnahmen, ausdrücklich ausgeschlossen wurden. Generell wäre es auch ratsam, die gleichzeitige Verabreichung dieser Medikamente mit jeder Art von Phosphatbindern zu vermeiden.
Sevelamer (Renagel®, Renvela®, Generikum Sevelámero)
Sevelamer ist ein nicht resorbierbares, vernetztes Polymer. Medikamente, die eine Verringerung ihrer Bioverfügbarkeit durch Sevelamer zeigen, sollten mindestens eine Stunde vor oder drei Stunden nach der Verabreichung von Sevelamer gegeben werden.19 Studien zu Arzneimittelinteraktionen bei gesunden Probanden ergaben, dass Sevelamerhydrochlorid die Bioverfügbarkeit von Ciprofloxacin um etwa 50 % verringert.20 Es ist sehr wichtig zu wissen, dass Sevelamer die Plasmaspiegel von Cyclosporin, Tacrolimus und Mycophenolatmofetil bei Transplantationspatienten verringern kann, obwohl dies keine offensichtlichen klinischen Folgen (z. B. Transplantatabstoßung) hat. Dennoch ist eine Überwachung ihrer Plasmaspiegel während der Anwendung dieser Kombination und nach deren Absetzen ratsam. Die TSH-Spiegel sollten bei Patienten, die Levothyroxin erhalten, überwacht werden (wie bei jedem Bindemittel). Sevelamer kann die Absorption der fettlöslichen Vitamine D, E, K und Folsäure vermindern, mit fraglicher klinischer Auswirkung.19 Im Gegensatz dazu hatte Sevelamer bei gesunden Probanden keinen Einfluss auf die Bioverfügbarkeit von so wichtigen Medikamenten wie Digoxin, Warfarin, Enalapril oder Metoprolol.21 Die gleichzeitige Verabreichung von Protonenpumpenhemmern mit Sevelamer kann jedoch in seltenen Fällen den Serumphosphatspiegel erhöhen.21
Lanthancarbonat (Fosrenol®)
Lanthan kann den pH-Wert im Magen erhöhen (ein ähnlicher Effekt wird bei Phosphatbindern auf Kalziumbasis beobachtet, die häufig in Kombinationen mit Antazida eingesetzt werden) und die orale Absorption von schwach basischen Arzneimitteln verringern. Es wird empfohlen, diese Verbindungen nicht zwei Stunden vor oder nach der Verabreichung von Lanthancarbonat einzunehmen (d. h. Antimalariamittel wie Chloroquin und Hydroxychloroquin, das Antimykotikum Ketoconazol oder Bisphosphonate).22 Die Bioverfügbarkeit von oralem Ciprofloxacin verringerte sich in einer Studie an gesunden Probanden um etwa 50 %, wenn es zusammen mit Lanthancarbonat verabreicht wurde.23 Im Gegensatz dazu hatte Lanthancarbonat keinen Einfluss auf die Serumkonzentrationen der fettlöslichen Vitamine A, D, E und K,24 obwohl kürzlich in vitro Wechselwirkungen mit Vitamin K2 beschrieben wurden.25 Es ist auch wichtig zu betonen, dass die Verabreichung von Lanthancarbonat bei gesunden Probanden das pharmakokinetische Profil von Digoxin, Warfarin, Metoprolol, Phenytoin oder Enalapril nicht veränderte.22
Sucroferric oxyhydroxide
Im Gegensatz zu anderen Phosphatbindern gibt es bei OHS keine Wechselwirkungen mit anderen Medikamenten (siehe Abbildung 1). Darüber hinaus wurde beschrieben, dass es in vitro keine relevanten Wechselwirkungen von OHS u. a. mit Cephalexin, Nifedipin und Chinidin gibt (Abbildung 1).26 Bei gesunden Probanden gibt es auch keine relevanten Wechselwirkungen mit Losartan, Furosemid, Omeprazol, Digoxin oder Warfarin.27 Bei Dialysepatienten interagiert OHS nicht mit Statinen (Atorvastatin und Simvastatin), obwohl vorläufige Daten in vitro die Möglichkeit einer solchen Wechselwirkung nahelegen. Im Gegensatz zu Sevelamer beeinflusst OHS nicht die hemmende Wirkung von oralem Vitamin D auf PTH28 und scheint im Gegensatz zu Lanthan nicht mit Vitamin K2 zu interagieren.25 Möglicherweise ist eine geringere orale Absorption von Medikamenten zu beobachten, die mit Eisen interagieren (wie Alendronat und Doxycyclin) oder, wie die anderen Bindemittel, mit Levothyroxin.29
Aluminiumbasierte Bindemittel
Obwohl in den KDIGO-Leitlinien empfohlen wird (Evidenz 1C), die längerfristige Anwendung von aluminiumbasierten Phosphatbindern zu vermeiden,2 stellt Abbildung 1 die vielfältigen Möglichkeiten von Wechselwirkungen entweder durch ihre potenzielle Verschreibung außerhalb unseres Geltungsbereichs oder als Masterformel dar.30 Wir müssen auch auf die Möglichkeit unbekannter Wechselwirkungen mit Immunsuppressiva oder neu entwickelten Medikamenten hinweisen.
Schlussfolgerung
Neben den beschriebenen potenziellen negativen Auswirkungen von calciumhaltigen Phosphatbindern sollten wir auch die größere Häufigkeit möglicher Arzneimittelinteraktionen mit vielen Medikamenten berücksichtigen, die routinemäßig bei unseren polymedizierten Patienten eingesetzt werden. Im Allgemeinen haben andere Bindemittel wie Sevelamer, Lanthan und OHS die Abwesenheit signifikanter Wechselwirkungen mit Medikamenten bewiesen, für die es bei den älteren Bindemitteln keine Informationen gibt. Ebenso sollte bedacht werden, dass jene Binder, die in der Monotherapie eine geringere Anzahl von Tabletten benötigen, nicht nur die Therapietreue verbessern, sondern auch das Risiko möglicher unerwünschter Wechselwirkungen verringern. Obwohl das Potenzial für Wechselwirkungen bei einigen Bindemitteln, insbesondere bei OHS, gering zu sein scheint, wäre es in jedem Fall ratsam, bei der Verwendung von Medikamenten mit einer engen therapeutischen Breite die Dosen zu trennen, um den klinischen Effekt zu erreichen und Nebenwirkungen zu reduzieren, sowohl zu Beginn der Behandlung als auch nach späteren Dosisanpassungen.
Erklärung der Autoren
Die Autoren stimmen der Einreichung des Artikels zur Veröffentlichung in der Zeitschrift Nefrologia zu und erklären, dass er nicht gleichzeitig an eine andere Zeitschrift zur Veröffentlichung geschickt wurde. Die Autoren erklären außerdem, dass es sich um eine Idee handelt, die nicht aus der pharmazeutischen Industrie stammt und dass ihr geistiges Eigentum an Nefrologia übertragen wird. Die Autoren genehmigen die endgültige Form und sind für den Inhalt verantwortlich.
Interessenkonflikte
J.B. hat Vortragshonorare von Abbvie, Amgen, Genzyme und Shire erhalten, und als Berater von Abbvie, Amgen, Vifor/Fresenius-Renal Pharma, Chugai, Medice und Genzyme/Sanofi. J.F.N.G. hat Vortrags- und/oder Beraterhonorare von Abbvie, Amgen, Astra-Zeneca, Boehringer-Ingelheim, Esteve, Genzyme, Sanofi, Servier, Shire und Vifor/Fresenius-Renal Pharma erhalten. M.D.A. hat Vorträge oder Beraterhonorare von Shire, Fresenius, Abbvie und Amgen erhalten. E.G.P. hat Beraterhonorare von Sanofi, Vifor/Fresenius-Renal Pharma, Amgen, Abbvie und Shire erhalten. A.L.M.F. erhielt Vortragshonorare von General Electric und Astra Zeneca sowie Beraterhonorare von Vifor/Fresenius-Renal Pharma. E.S. hat Vortragshonorare von Abbvie, Sanofi, Shire, Vifor/Fresenius-Renal Pharma erhalten. A.M.M. hat Vortragshonorare von Abbvie, Amgen, Shire, Bellco, Fresenius-Medical Care erhalten. M.J.Ll. erhielt Vortragshonorare von Sanofi und Abbvie, sowie Beraterhonorare von Vifor/Fresenius-Renal Pharma. P.M.V. erhielt Vortragshonorare von Amgen, Sanofi und Vifor/Fresenius-Renal Pharma und Beraterhonorare von Vifor/Fresenius-Renal Pharma. M.A.B. hat Vortragshonorare von Vifor/Fresenius-Renal Pharma erhalten. I.D. hat Honorare für die wissenschaftliche Zusammenarbeit mit Vifor/Fresenius-Renal Pharma erhalten.