US Pharm. 2017;42(12):HS2-HS6.
ABSTRACT: La diarrea è spesso il sintomo rivelatore nei pazienti affetti da sindrome carcinoide secondaria a un tumore carcinoide. Si pensa che l’eziologia di questa diarrea pesante sia l’ipersecrezione di serotonina dalle cellule neuroendocrine. La diagnosi viene fatta sulla base dei sintomi clinici e di due biomarcatori, l’acido 5-idrossiindoleacetico (trovato nelle urine) e la cromogranina A (trovata nel siero). Gli analoghi sintetici della somatostatina (SSA) sono stati un punto fermo della terapia per anni e continuano ad essere utilizzati. Telotristat è il primo farmaco orale indicato in combinazione con gli SSA per i pazienti con diarrea da sindrome carcinoide che non rispondono più ai soli SSA.
I tumori neuroendocrini (NET) comprendono un’ampia varietà di tumori a crescita lenta. L’incidenza negli Stati Uniti varia da due a cinque per 100.000 pazienti e sembra essere in aumento, probabilmente a causa di migliori tecniche di screening.1 Anche se questi tumori sono generalmente asintomatici, i sintomi sono più probabilità di sviluppare quando un tumore metastatizza al fegato o al polmone o se il tumore primario ha origine midgut-i.e, intestino tenue, appendice o intestino crasso prossimale.2,3
Tumori carcinoidi e sindrome carcinoide
I tumori carcinoidi sono NET che nascono principalmente dalle cellule enterochromaffini situate nel tratto gastrointestinale (GI) e bronchiale.1,2 Queste cellule sono responsabili della produzione, stoccaggio e secrezione di molte sostanze biologicamente attive – tra cui serotonina, noradrenalina, dopamina, istamina, bradichinina, prostaglandine, sostanza P e altre – che possono portare allo sviluppo della sindrome carcinoide, un termine collettivo che comprende una varietà di sintomi mediati dagli ormoni secreti dal tumore carcinoide.1-4
Un NET ben differenziato esprime numerosi recettori della somatostatina (SSTR).1 Dei cinque tipi di SSTR, SSTR1 e SSTR5 sono presi di mira dagli analoghi sintetici della somatostatina (SSA). I tumori carcinoidi producono un eccesso di serotonina, che esaurisce il triptofano endogeno. Una cellula normale converte solo l’1% del triptofano in serotonina, mentre una cellula tumorale carcinoide produce serotonina finché le riserve di triptofano non sono esaurite.3 Il triptofano è un precursore della niacina, che è un componente essenziale della nicotinamide e della nicotinamide adenina dinucleotide/nicotinamide adenina dinucleotide fosfato, così come della sintesi proteica.3
I sintomi più comuni della sindrome carcinoide sono vampate, diarrea, tachicardia, broncospasmo e mancanza di respiro. Anche l’instabilità emodinamica può verificarsi, sebbene ciò sia raro con le terapie attuali.5 I pazienti con una sindrome da carcinoide incontrollata a lungo termine possono sviluppare pellagra, lesioni valvolari cardiache, teleangectasia venosa e/o broncospasmo.2 Meno del 10% dei pazienti con tumori carcinoidi GI sviluppano una sindrome da carcinoide, e la maggior parte di quelli che lo fanno hanno metastasi epatiche.2
Diarrea da sindrome carcinoide
La diarrea si verifica nell’80% dei pazienti con sindrome carcinoide.6 I pazienti con diarrea da sindrome carcinoide presentano feci esplosive, acquose e molli più volte al giorno, il che può essere pesante per il paziente e impegnativo per l’operatore sanitario. Uno studio di coorte ha rilevato che i costi sanitari sono 1,5 volte superiori e il rischio di ospedalizzazione è due volte superiore nei pazienti con diarrea da sindrome da carcinoide rispetto a quelli senza diarrea.7 La fisiopatologia della diarrea da sindrome da carcinoide comporta la presenza di un eccesso di serotonina, che stimola la secrezione di muco colonico, aumenta la peristalsi e inibisce l’assorbimento nel tratto GI, che porta alla diarrea.3,4,6 Rispetto ai pazienti sani, il tempo di transito del colon prossimale può essere fino a sei volte più veloce e il tempo di transito dell’intestino tenue può essere due volte più veloce nei pazienti con diarrea da sindrome carcinoide.6
Fattori di rischio
Si pensa che i NET si sviluppino sporadicamente o in individui geneticamente predisposti.3 Quando un parente di primo grado ha un NET, la probabilità di sviluppare un NET è 12,5 su 100.000 persone e 15,7 su 100.000 persone per uomini e donne, rispettivamente.7 Altre condizioni associate, riportate in una revisione retrospettiva di 36 pazienti con diarrea da sindrome carcinoide, includono gastrite atrofica (67%), anemia perniciosa (58%), ipotiroidismo (39%), diabete (19%), insufficienza adrenocorticale (6%) e iperparatiroidismo (6%).8 Secondo un’indagine prospettica su 494.000 soggetti iscritti al NIH-AARP Diet and Health Study e seguiti per 8 anni, l’assunzione di grassi saturi è associata a un aumento del rischio di sviluppare tumori carcinoidi.9 Le assunzioni di carne e grassi sono stati stimati da questionari di frequenza alimentare. Il rischio di tumori carcinoidi dell’intestino tenue era associato a un’elevata assunzione di grassi saturi rispetto a una bassa assunzione di grassi saturi (hazard ratio 3.18; 95% CI, 1.62-6.25).9 Una volta che un paziente ha diarrea da sindrome carcinoide, la dieta e lo stress possono influire sui sintomi. I pazienti devono evitare i fattori precipitanti come gli alimenti che contengono tirosina (formaggio stagionato, carne e pesce fermentati, cibi in salamoia, tofu, cioccolato), l’alcol e l’aumento delle catecolamine (esercizio, sforzo).1,2
Diagnosi
La diagnosi della diarrea da sindrome carcinoide si basa sui sintomi di diarrea e vampate di calore combinati con i risultati oggettivi del tumore carcinoide attraverso la biopsia, la TAC addominale/pelvica multifase, la risonanza magnetica o i biomarcatori.10 I biomarcatori acido 5-idrossiindoleacetico (5-HIAA; si trova nelle urine) e cromogranina A (CgA; si trova nel siero) hanno una specificità e una sensibilità accettabili per i tumori carcinoidi.10,11 La serotonina viene metabolizzata dalla monoamino ossidasi in 5-HIAA, e la CgA viene rilasciata dalle pareti delle vescicole che immagazzinano serotonina. I livelli normali di 5-HIAA nelle urine vanno da 3 a 15 mg/24 h; un livello elevato ha una specificità del 100% e una sensibilità del 73% per i tumori carcinoidi.11 I livelli sierici di CgA tendono a correlarsi con la massa tumorale, ma non con i sintomi. Livelli di CgA superiori a 130 mcg/L sono associati al 98,4% di specificità e al 62,9% di sensibilità per i tumori carcinoidi.11 I pazienti dovrebbero evitare cibi ricchi di serotonina 48 ore prima della raccolta delle urine. I livelli urinari di 5-HIAA possono essere falsamente abbassati dalla levodopa, mentre i livelli sierici di CgA possono essere falsamente elevati dagli inibitori della pompa protonica, dall’insufficienza renale o da condizioni infiammatorie.10-13
Trattamento
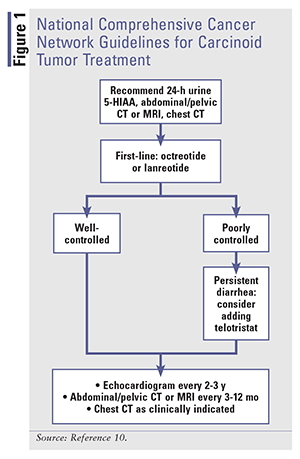
Le modalità di trattamento della diarrea da sindrome carcinoide si concentrano sul miglioramento dei sintomi e sulla modifica della malattia stessa, come evidenziato dalla normalizzazione dei biomarcatori.11 Gli SSA sono il pilastro della terapia per i tumori carcinoidi. La somatostatina influenza diverse funzioni gastrointestinali, tra cui la motilità gastrointestinale, la secrezione di ormoni pancreatici e intestinali e la secrezione della bile e dei liquidi del colon.13 Quando si lega ai recettori, la somatostatina inibisce la secrezione di mediatori biologici, il che migliora notevolmente le vampate e la diarrea abbassando la serotonina, come dimostrato dalla riduzione della 5-HIAA nelle urine.13 La regressione del tumore si osserva anche con gli SSA.12,14,15 Vedere la FIGURA 1 per le linee guida del National Comprehensive Cancer Network (NCCN) per il trattamento dei tumori carcinoidi.
Somatostatin Analogues: Gli SSA octreotide e lanreotide forniscono il controllo ormonale nei pazienti con tumori carcinoidi.16,17 L’octreotide a breve durata d’azione (SA) è stato il primo SSA approvato per il controllo dei sintomi associati ai tumori carcinoidi.16,18 Purtroppo, con un’emivita di 2 ore, è necessario un dosaggio ripetuto. L’ottreotide a rilascio prolungato (LA) fornisce livelli sostenuti di farmaco e viene somministrato mensilmente per via IM.15 Gli studi che confrontano le formulazioni SA e LA hanno dimostrato un’efficacia simile in termini di controllo dei sintomi, con tassi di risposta dal 60% al 72%.18
Lanreotide è disponibile in una formulazione a rilascio prolungato (Somatuline Depot) somministrata mediante iniezione SC profonda ogni 4 settimane.17,18 SA octreotide e LA lanreotide hanno un’efficacia simile nel fornire sollievo dai sintomi.16 È stato condotto uno studio clinico di fase III per valutare l’uso di SA octreotide SC per controllare i sintomi associati alla sindrome carcinoide in pazienti che ricevevano lanreotide 120 mg SC (n = 59) o placebo (n = 56) ogni 4 settimane per 16 settimane.19 La percentuale di giorni con octreotide come farmaco di salvataggio era significativamente più bassa nei pazienti con lanreotide (33,7%; 95% CI, 25%-42,4%) rispetto ai pazienti con placebo (48,5%; 95% CI, 39,6%-57,4%, P = .016).
Pasireotide (Signifor) si lega a SSTR1 e SSTR5 con un’affinità maggiore di octreotide e lanreotide.16 In uno studio clinico di fase II, ha dimostrato efficacia in pazienti con NET avanzati e sindrome carcinoide che non rispondevano più all’octreotide.20 Pasireotide a rilascio prolungato (LAR), approvato dalla FDA solo per l’acromegalia e la sindrome di Cushing, ha dimostrato un’efficacia simile nel controllo dei sintomi della sindrome carcinoide rispetto all’octreotide LAR ad alte dosi e ha portato a una migliore sopravvivenza libera da progressione nei pazienti refrattari agli SSA in uno studio di fase III del 2015.21,22
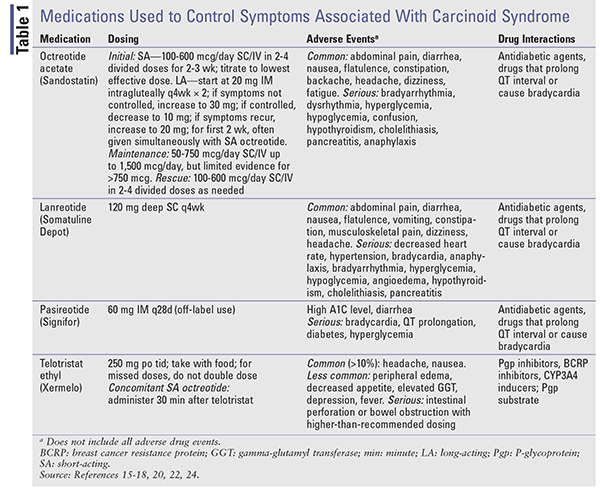
Quando il controllo dei sintomi è l’obiettivo, la terapia inizia con octreotide SA. Poiché possono essere necessarie fino a 3 settimane perché le preparazioni LA raggiungano livelli di stato stazionario, il controllo dei sintomi può essere gestito con SA octreotide.15,18 Il dosaggio viene iniziato basso (100-600 mcg al giorno in 2-4 dosi) e viene titolato alla dose efficace più bassa necessaria per controllare i sintomi. LA octreotide inizia a 20 mg IM intraglutealmente ogni 4 settimane, con SA octreotide somministrato in concomitanza per almeno 2 settimane. Vedere la TABELLA 1 per il dosaggio, gli eventi avversi e le potenziali interazioni farmaco-farmaco.
Telotristat etile: Telotristat etile (Xermelo), che è un prodrug del telotristat, inibisce l’enzima triptofano idrossilasi, portando ad una diminuzione della serotonina periferica. È approvato dalla FDA per il trattamento della diarrea da sindrome carcinoide in combinazione con la terapia SSA in pazienti non adeguatamente controllati dalla sola terapia SSA.23,24 È stato condotto uno studio prospettico e randomizzato di fase III in cui 135 pazienti con quattro o più movimenti intestinali al giorno nonostante la SSA a dose stabile hanno ricevuto telotristat 250 mg tre volte al giorno, telotristat 500 mg tre volte al giorno o placebo per 12 settimane.25 Le riduzioni medie della frequenza giornaliera dei movimenti intestinali per placebo, telotristat 250 mg e telotristat 500 mg erano rispettivamente -0,9, -1,7 e -2,1. Telotristat è costoso, con un prezzo medio all’ingrosso di 6.196,80 dollari per ottantaquattro compresse da 250 mg.23
Altri agenti: La diarrea da sindrome carcinoide viene trattata con gli SSA, e il telotristat viene aggiunto quando i sintomi rimangono incontrollati. Una risposta positiva agli agenti chemioterapici che trattano il NET sottostante, riducendo così l’attività del tumore, può alleviare i sintomi della sindrome da carcinoide. Va oltre lo scopo di questo articolo esaminare questi agenti chemioterapici. Se la malattia progredisce dopo l’uso di octreotide o lanreotide, l’NCCN raccomanda l’uso di everolimus; interferone alfa-2b; o gli agenti chemioterapici citotossici 5-fluorouracile, capecitabina, dacarbazina, oxaliplatino, streptozocina, o temozolomide per NET non resecabili e/o metastatici del tratto gastrointestinale.10
Conclusione
L’incidenza dei tumori carcinoidi, un tipo di NET, è in aumento. Non sono noti fattori di rischio per lo sviluppo dei NET o fattori che possano identificare quali pazienti svilupperanno la sindrome da carcinoide, anche se la maggior parte dei pazienti con sindrome da carcinoide ha spesso metastasi al fegato all’esordio. La sindrome carcinoide descrive un gruppo di sintomi mediati da vari ormoni rilasciati da un tumore carcinoide. Non tutti i pazienti con tumori carcinoidi sperimentano la sindrome da carcinoide. La diarrea da sindrome da carcinoide può essere esplosiva e può verificarsi più volte al giorno. Gli SSA sono il pilastro della terapia per il sollievo sintomatico della diarrea secondaria ai tumori carcinoidi, e le nuove terapie, come il telotristat aggiunto alla terapia SSA, forniscono opzioni per i pazienti i cui sintomi sono insopportabili.
1. Cives M, Soares HP, Strosberg J. L’eterogeneità clinica dei tumori neuroendocrini avrà un impatto sulla loro gestione in futuro? Lezioni da studi recenti. Curr Opin Oncol. 2016;28:359-366.
2. Robertson RG, Geiger WJ, Davis NB. Tumori carcinoidi. Am Fam Physician. 2006;74:429-434.
3. Lips CJ, Lentjes EG, Höppener JW. Lo spettro dei tumori carcinoidi e delle sindromi carcinoidi. Ann Clin Biochem. 2003;40:612-627.
4. Bertrand PP, Bertrand RL. Rilascio e assorbimento della serotonina nel tratto gastrointestinale. Auton Neurosci. 2010;153:47-57.
5. Yao JC, Hassan M, Phan A, et al. Cento anni dopo il “carcinoide”: epidemiologia e fattori prognostici per i tumori neuroendocrini in 35.825 casi negli Stati Uniti. J Clin Oncol. 2008;26:3063-3072.
6. von der Ohe MR, Camilleri M, Kvols LK, Thomforde GM. Disfunzione motoria dell’intestino tenue e del colon in pazienti con la sindrome carcinoide e diarrea. N Engl J Med. 1993;329:1073-1078.
7. Babovic-Vuksanovic D, Constantinou CL, Rubin J, et al. Occorrenza familiare di tumori carcinoidi e associazione con altre neoplasie maligne. Cancro Epidemiol Biomarkers Prev. 1999;8:715-719.
8. Gough DB, Thompson GB, Crotty TB, et al. Diverse caratteristiche cliniche e patologiche del carcinoide gastrico e la rilevanza dell’ipergastrinemia. World J Surg. 1994;18:473-479.
9. Croce A, Leitzmann MF, Subar AF, et al. Uno studio prospettico dell’assunzione di carne e grassi in relazione al cancro del piccolo intestino. Cancer Res. 2008;68:9274-9279.
10. National Comprehensive Cancer Network. Linee guida di pratica clinica NCCN in oncologia (NCCN guidelines®): tumori neuroendocrini. Versione 3.2017. www.nccn.org/professionals/physician_gls/PDF/neuroendocrine.pdf. Accessed October 11, 2017.
11. Maroun J, Kocha W, Kvols L, et al. Linee guida per la diagnosi e la gestione dei tumori carcinoidi. Parte 1: il tratto gastrointestinale. Una dichiarazione di un gruppo nazionale canadese di esperti di carcinoidi. Curr Oncol. 2006;13:67-76.
12. Eriksson B, Oberg K, Stridsberg M. Marcatori tumorali nei tumori neuroendocrini. Digestione. 2000;62(suppl 1):33-38.
13. van der Lely AJ, de Herder WW. Sindrome carcinoide: diagnosi e gestione medica. Arq Bras Endocrinol Metabol. 2005;49:850-860.
14. Cives M, Strosberg J. Strategie di trattamento per i tumori neuroendocrini metastatici del tratto gastrointestinale. Curr Treat Options Oncol. 2017;18:14.
15. Enzler T, Fojo T. Analoghi della somatostatina a lunga durata d’azione nel trattamento dei tumori neuroendocrini non resecabili/metastatici. Semin Oncol. 2017;44:141-156.
16. Octreotide. Lexicomp Online. Hudson, OH: Lexi-Comp, Inc; 2017. http://online.lexi.com. Accessed October 11, 2017.
17. Lanreotide. Lexicomp Online. Hudson, OH: Lexi-Comp, Inc; 2017. http://online.lexi.com. Accessed October 11, 2017.
18. Narayanan S, Kunz PL. Ruolo degli analoghi della somatostatina nel trattamento dei tumori neuroendocrini. Hematol Oncol Clin N Am. 2016;30:163-177.
19. Vinik AI, Wolin EM, Liyanage N, et al. Valutazione di lanreotide depot/autogel efficacia e sicurezza come trattamento della sindrome di carcinoide (ELECT): uno studio randomizzato, in doppio cieco, controllato con placebo. Endocr Pract. 2016;22:1068-1080.
20. Kvols LK, Oberg KE, O’Dorisio TM, et al. Pasireotide (SOM230) mostra efficacia e tollerabilità nel trattamento di pazienti con tumori neuroendocrini avanzati refrattari o resistenti a octreotide LAR: risultati di uno studio di fase II. Endocr Relat Cancer. 2012;19:657-666.
21. Wolin EM, Jarzab B, Eriksson B, et al. Studio di fase III di pasireotide a rilascio prolungato in pazienti con tumori neuroendocrini metastatici e sintomi carcinoidi refrattari agli analoghi della somatostatina disponibili. Drug Des Devel Ther. 2015;9:5075-5086.
22. Pasireotide. Soluzioni Micromedex. Greenwood Village, CO: Truven Health Analytics. www.micromedexsolutions.com. Accessed October 23, 2017.
23. Markham A. Telotristat etile: prima approvazione globale. Farmaci. 2017;77:793-798.
24. Telotristat. Lexicomp Online. Hudson, OH: Lexi-Comp, Inc; 2017. http://online.lexi.com. Accessed October 11, 2017.
25. Kulke MH, Hörsch D, Caplin ME, et al. Telotristat etile, un inibitore della triptofano idrossilasi per il trattamento della sindrome carcinoide. J Clin Oncol. 2017;35:14-23.