食道運動障害は、しばしば軽視される疾患です。
食道運動障害は、胸焼け、胸痛、慢性咳などの非特異的な臨床症状が他の一般的な疾患と重なることが多いだけでなく、食道機能を検査する機器も不足しています。 2001年、SpechlerとCastell1はこれらのデータを応用して、食道マノメトリー障害を次の4つのグループに分類することを提案した:
1.
1.下部食道括約筋(LES)の不十分な弛緩:古典的なアカラシアや非典型的なLESの弛緩障害の可能性がある。
2.食道体部の不調和な収縮:びまん性食道痙攣の可能性がある。
3.食道体部(くるみ割り食道)やLES(高血圧性LES)で起こる食道の過収縮。
4.食道体部低収縮(IEM)
1991年、Clouseら2は従来のマノメトリック検査から食道トポグラフを作成することを開始し、食道運動障害の診断精度が向上したことを明らかにした3。 2007年にサンディエゴで開催されたDDWミーティングでは、高解像度マノメトリ(HRM)ワーキンググループが、臨床的な食道運動機能障害を評価するために食道内圧トポグラフィ(EPT)を調整することに初めて協力した。 2008年、Kahrilasら4は、食道運動障害の診断に食道内圧トポグラフィを用いた初のChicago classifcation(CC)を発表し、その後、2012年にCCバージョン2.0、2015年にCCバージョン3.0が発表されました5,6
CCバージョン3.0によると、食道運動障害は主に以下のように分類されます。
1.LESの弛緩不良(アカラシアや食道胃接合部(EGJ)流出障害の可能性あり)
2.蠕動運動の主要な障害:収縮力の欠如、遠位食道
痙攣、ジャックハンマー食道
3.蠕動運動のマイナーな障害。 IEMまたは断片化された蠕動運動6。
CCバージョン1.04で言及された高血圧(呼気終末安静時LES圧< 10 mmHg、正常な蠕動運動を伴う)と高血圧性LES(呼気終末安静時LES> 35 mmHg、正常な蠕動運動とEGJ弛緩を伴う)の両方は、バージョン2.0と3.0.5ではさらに発行されていません。
アカラシア
特発性アカラシアは、食道の蠕動運動の低下とLESの弛緩障害を特徴とする原発性食道疾患である7。 アカラシアが疑われる患者の約3-4%は偽アカラシアである8。偽アカラシアとは、悪性細胞が食道遠位部やEGJの腸神経叢に炎症を起こし、破壊している場合に起こる症状である。 特発性アカラシアは稀な疾患である。 発症率は成人10万人あたり年間0.3~1.63人、有病率は10年間で成人10万人あたり8.7~11.2人となっています。
アカラシアの病因は、腸管神経叢の後神経節抑制ニューロンの機能低下または消失である。後神経節抑制ニューロンは、血管作動性腸管ポリペプチド(VIP)と一酸化窒素(NO)の2つの神経伝達物質を分泌して、食道遠位部およびEGJの平滑筋に供給している15, 16。 特にHLA DQA1*0103やHLA DQB1*0603を持つ患者では、細胞傷害性リンパ球や補体の活性化がこの慢性神経節炎の原因となる可能性がある18。 特発性アカラシアの臨床症状は食道疾患の程度と相関していると考えられている。 食道筋神経炎や神経節炎の患者は、最初は勢いのあるアカラシア(III型アカラシア)を呈することがほとんどである。 17
アカラシア患者の90%以上が固形物や液体の嚥下障害を呈すると言われている。 その他の症状としては、胸焼け、未消化物の逆流、非心臓性の胸痛、体重減少などがあります。 19, 20 食道胃十二指腸内視鏡検査(EGD)は、機械的閉塞を除外するために、嚥下障害のある患者に実施すべきであるが、アカラシアの診断には、特に早期の段階では感度が低い19。 アカラシアに見られるEGD所見は、食道の拡張や蛇行、食道内腔の食物の滞留、食道カンジダ症、胃カメラをEGJに通す際の若干の抵抗感などである20
バリウム食道造影もアカラシアの初期段階の判定には感度が低いとされている。 特発性アカラシアでは食道拡張やbird-beakの外観が認められることがある。 慎重には、遠位の食道狭窄の長さが3.5cm以上で、近位の食道拡張が4cm以下の場合は、医師は偽性アカラシアを疑うべきである21。
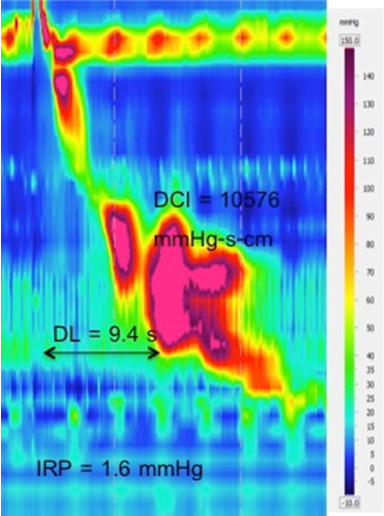
現在のCCバージョン3.0によると、アカラシアは3つのタイプに分類されている。 I型アカラシアの診断基準は、EGJの弛緩障害と100%失敗した蠕動運動である(図7)。 断層性蠕動運動とは、少なくとも50%以上の断片的な収縮を呈する状態である(DCI > 450 mmHg-s-cmで、20mmHg等圧線上にブレイク > 5cmの長さがあるツバメ)(図7)。6 これらの食道運動機能低下症はいずれもLESが正常に弛緩していることが必要である。
現在、食道蠕動運動を回復させるための食道運動機能低下症の治療法はまだ限られている。 69 生活習慣の改善は、食道ボーラスの通過性を向上させ、食道の酸曝露を減少させる。69 食物をよく噛むこと、液体や半固体の食物を摂取すること、多量の水を飲むこと、炭酸飲料を使用することは、食道ボーラスの通過性を向上させ、ボーラスの貯留を防ぐことができる。 体重を減らすこと、食後すぐに仰向けになることを避けること、ベッドの頭を高くすること、左側臥位をとること、油分の多い食品や高カロリーの食事を避けることは、食道の酸曝露や再燃症状の頻度を減らすのに有効である78, 79 さらに、ガムを噛むことで、GERD患者の食道酸曝露量が減少し、再燃症状が緩和されることを示す研究がいくつかある80-82。
食道低収縮症患者に対する薬物療法としては、酸分泌抑制療法、酸および非酸の再還流を抑制するアルギン酸形成胃内ラフト、ドンペリドン、メトクロプラミド、マクロライド、セロトニン受容体アゴニストおよび/またはアンタゴニストなどのプロキネティックなどがある69。 84,85
結論として、LES機能障害や食道蠕動運動異常などの食道運動障害は重要な疾患である。 しかし、日常診療でよく見られるGERDと重なる臨床症状もあるため、過小評価されがちである。 さらに、食道内圧検査は広く普及しておらず、一般の医師はこの高度な食道機能検査に精通していないかもしれない。 原因不明の難治性食道症状(胸焼け、逆流、非心臓性胸痛など)や呼吸器症状(慢性咳嗽など)を有する患者に食道内圧検査を行うことで、特異な食道運動障害が明らかになるかもしれない。