Właściwości związków jonowych
Ponieważ wszystkie związki jonowe powstają, gdy aniony i kationy są przyciągane do siebie, związki jonowe często mają podobne właściwości.
Związki jonowe tworzą kryształy
Związki jonowe składają się z kationów i anionów, które przylegają do siebie z powodu ich przeciwnych ładunków. Wyobraź sobie pojedynczy kation litu, który przylega do pojedynczego anionu chloru, tworząc chlorek litu. Jest mało prawdopodobne, że tylko jeden jon litu i jeden jon chlorku będą obecne w tym miejscu? Ogólnie rzecz biorąc, kiedy mówimy o reakcjach chemicznych, mówimy o ogromnej liczbie atomów przechodzących reakcję w bardzo małym miejscu (jedna łyżeczka soli zawiera około 1022 atomy). W rezultacie, gdyby nasza pojedyncza para LiCl zbliżyła się do innej pary LiCl, miałoby miejsce następujące zjawisko:
Ponieważ przeciwnie naładowane jony przyciągają się wzajemnie, pary LiCl będą miały tendencję do tworzenia większych grup. Te większe grupy, z kolei, będą tworzyć jeszcze większe grupy jonów, jak pokazano na poniższym rysunku:
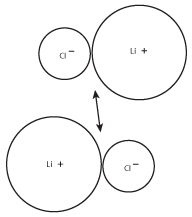
Rysunek 8.3Pozytywny ładunek na kationie litu jednej pary będzie przyciągany do ujemnego ładunku na jonie chlorkowym drugiej pary.

Rysunek 8.4Ten proces, w którym stosy jonów LiCl łączą się ze sobą, będzie trwał aż do momentu, gdy nie będzie już więcej jonów litu lub chlorku.
Kryształy to duże układy jonów lub atomów, które są ułożone w regularne wzory. Wiele związków jonowych tworzy bardzo duże kryształy.
Te duże układy jonów są określane jako kryształy. Chociaż kryształy są często tworzone ze związków jonowych, istnieją one również w niektórych innych związkach chemicznych, takich jak diamenty. Porozmawiamy o tym bardziej szczegółowo w Solids.
Hydraty są tworzone, gdy jedna lub więcej cząsteczek wody przyłącza się do związków jonowych. Związki te są interesujące, ponieważ wydają się suche, ale po podgrzaniu wydzielają wodę. Szczególnie interesująca jest sól Epsom, czyli heptahydrat siarczanu magnezu (MgSO47H2O). Po podgrzaniu wydziela się tyle wody, że faktycznie rozpuszcza siarczan magnezu!
Związki jonowe często mają wysokie temperatury topnienia i wrzenia
Co się dzieje, gdy podgrzejesz coś w kuchni? Być może odkryłeś podczas gotowania (lub podczas mikrofalowania przypadkowych rzeczy podczas nudy), że większość żywności, którą jemy, topi się lub pali po podgrzaniu. Niektóre produkty potrafią nawet zrobić jedno i drugie! Jak pewnie się domyślasz, jestem ekspertem jeśli chodzi o gaszenie pożarów w domu.
Związki jonowe, z drugiej strony, często topią się i gotują w znacznie wyższych temperaturach niż inne materiały. Aby związki jonowe mogły się topić, należy dodać wystarczająco dużo energii, aby kationy i aniony oddaliły się od siebie. Ponieważ te przyciągania są tak silne, potrzeba dużo energii, aby odciągnąć te jony od siebie. Dodanie takiej ilości energii do związków jonowych wymaga dużej ilości ciepła, dlatego związki jonowe mają bardzo wysokie temperatury topnienia i wrzenia.
Związki jonowe są twarde i kruche
Wyobraź sobie, że uderzasz dużym kawałkiem chlorku litu o swoją głowę. Jak przypuszczasz, jakie to może być uczucie? Jeśli zgadłeś, że będzie bolało jak szalone, to miałeś rację. Podobnie jak wiele związków jonowych, chlorek litu jest twardy jak skała.
Związki jonowe są niezwykle twarde, ponieważ trudno jest sprawić, by jony oddaliły się od siebie w krysztale. Nawet jeśli przyłożysz dużą siłę do kryształu (wyobraź sobie, że wbiegasz głową w gigantyczną ścianę chlorku litu), przyciąganie między kationami i anionami często będzie nadal utrzymywać kryształ razem.
Powiedzmy jednak, że naprawdę chcesz rozbić związek jonowy. Chociaż bardzo twarde, związki jonowe są również często bardzo kruche, co oznacza, że rozpadają się, gdy przyłożona jest odpowiednia siła. Jak pokazuje poniższy rysunek, miejsce przyłożenia siły jest tak samo ważne jak jej ilość.

Rysunek 8.5Przykładając siłę w sposób, który odsuwa od siebie kationy i aniony: można spowodować całkowite rozpadnięcie się kryształu.
Jak widać z tego diagramu, kryształy jonowe ustawiają się w taki sposób, że istnieją regiony, w których niewielka siła może rozerwać kryształ. Te regiony są czasami nazywane „płaszczyznami rozszczepienia”, ponieważ są to miejsca, w których kryształ jest najsłabszy i może być najłatwiej złamany.
Związki jonowe przewodzą prąd elektryczny, gdy są rozpuszczone w wodzie lub stopione
W pewnym czasie był wynalazca, który wymyślił urządzenie do suszenia włosów. Ta „suszarka”, jak ją nazywał, ogrzewała powietrze elektrycznością i dmuchała na włosy osoby trzymającej ją w ręku. Ponieważ woda paruje pod wpływem ciepła, włosy schły szybciej. Dziedzictwo tego wynalazcy żyje po dziś dzień w urządzeniu domowym uwielbianym przez miliony.
Elektrolity to związki, które przewodzą prąd elektryczny po rozpuszczeniu w wodzie. Wiele związków jonowych jest uważanych za elektrolity. Jednakże, niektóre związki jonowe nie rozpuszczają się w wodzie. W rezultacie nie dzielą tej właściwości.
Krótko potem był facet, który zdecydował, że nie chce czekać, aby wyjść z wanny przed wysuszeniem włosów. Jego spuścizna: Naklejka ostrzegawcza suszarki do włosów z obrazkiem faceta porażonego prądem.
Gdy związki jonowe są umieszczone w wodzie, powodują, że woda przewodzi prąd. Normalnie, woda nie przewodzi elektryczności dobrze w ogóle. Jednak, gdy sole rozpuszczają się w wodzie, rozpadają się na swoje składowe kationy i aniony i to właśnie obecność tych jonów pozwala jej przewodzić prąd. Ponieważ sole przewodzą elektryczność, gdy są rozpuszczone w wodzie, są one określane jako elektrolity.
W ten sam sposób czyste sole przewodzą elektryczność, gdy są stopione. Jako ciało stałe, aniony i kationy w związku jonowym są zablokowane w miejscu i nie są w stanie przenieść ładunku elektrycznego. Jednakże, gdy związek jonowy jest topiony, te jony są wolne, aby poruszać się i przewodzić ładunek.
Wyciąg z The Complete Idiot’s Guide to Chemistry 2003 przez Ian Guch. Wszystkie prawa zastrzeżone, łącznie z prawem reprodukcji w całości lub w części w jakiejkolwiek formie. Used by arrangement with Alpha Books, a member of Penguin Group (USA) Inc.
Aby zamówić tę książkę bezpośrednio od wydawcy, odwiedź stronę Penguin USA lub zadzwoń pod numer 1-800-253-6476. Możesz również kupić tę książkę w Amazon.com i Barnes & Noble.