Faits clés & Résumé:
- L’enthalpie du réseau est une mesure de la force des forces entre les ions dans un solide ionique.
- L’énergie de réseau est l’énergie nécessaire pour séparer 1 mol d’un solide ionique en ions gazeux
- L’enthalpie de réseau augmente avec les charges et diminue avec la taille des ions.
- Le cycle de Born-Haber représente une série d’étapes menant à la formation d’un composé ionique à partir des ions gazeux qui le constituent
D’abord, qu’est-ce que le réseau ?
En chimie, lorsque le terme treillis est utilisé, nous faisons généralement référence à un treillis cristallin qui est une substance très transparente avec une forme géométrique régulière. L’arrangement tridimensionnel des atomes ou des ions dans un motif cristallin organisé à l’intérieur est appelé réseau cristallin. Par exemple, si nous disons » réseau cristallin de chlorure de sodium « , nous entendons un motif géométrique régulier d’ions sodium et chlorure.
L’enthalpie de réseau est généralement applicable aux composés ioniques, qui sont des composés formés par des métaux et des non-métaux. Les valeurs d’enthalpie de réseau (H) sont généralement représentées en kilojoules (KJ). L’enthalpie de réseau et l’énergie de réseau sont couramment utilisées comme si elles signifiaient exactement la même chose, bien qu’il existe une différence entre elles qui concerne les conditions dans lesquelles elles sont calculées.
L’énergie de réseau est l’énergie nécessaire pour séparer 1 mole d’un solide ionique en ions gazeux.
Si nous prenons NaCl comme exemple et que nous voulons préparer un réseau cristallin de chlorure de sodium, l’enthalpie de réseau du chlorure de sodium sera l’énergie nécessaire pour former un cristal de chlorure de sodium solide à partir d’ions sodium et chlorure gazeux.
La formation d’un cristal solide libère généralement une énorme quantité d’énergie dans l’environnement ; par conséquent, le processus est exothermique, et sa valeur est donc toujours négative.
Na (s) +1 Cl2 → NaCl (s) ΔH = – 411KJ
L’enthalpie de réseau est une mesure de la force des forces entre les ions dans un solide ionique. Plus l’enthalpie de réseau est grande, plus les forces sont fortes, et plus l’énergie libérée dans l’environnement lors de la formation du cristal est élevée. Cette énergie est libérée lorsque des liaisons sont établies et est nécessaire pour rompre les liaisons. Cette force cesse d’exister uniquement lorsque le sel est à l’état gazeux, donc lorsque les ions sont dispersés trop loin les uns des autres.
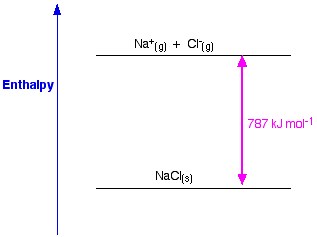
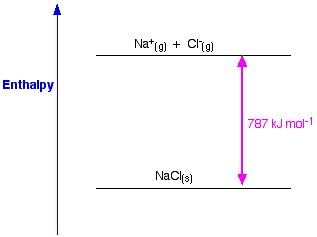
Figure 1. Enthalpie de réseau de NaCl. Www.chemguide.co.uk.
Les principaux facteurs affectant l’enthalpie de réseau sont la charge des ions et les rayons des ions. Analysons-les un par un.
Charges des ions
Plus les charges des ions sont importantes, plus les attractions entre eux sont grandes, et par conséquent plus l’enthalpie de réseau est grande. Par exemple, le chlorure de sodium NaCl et l’oxyde de magnésium MgO ont exactement les mêmes arrangements d’ions, mais les enthalpies de réseau sont très différentes. Comme le Mg a 2 charges positives +2, elles attirent les charges négatives O -2 plus que la charge de Na + 1 n’attirant qu’une seule négative Cl – 1 .
Les rayons des ions
Plus le rayon des ions est petit, plus les charges sont proches, plus l’attraction entre elles est grande et par conséquent plus l’enthalpie de réseau est grande. Par conséquent, plus la taille des ions augmente, plus l’énergie de maille diminue. En utilisant l’échantillon ci-dessus, l’enthalpie de MgO est également beaucoup plus grande que celle de NaCl car l’atome de Mg est plus petit que Na et l’atome d’O est plus petit que Cl.
L’énergie de la maille diminue donc vers le bas d’un groupe sur le tableau périodique.
Vous trouverez ci-dessous une image très utile du tableau périodique et des tendances de toutes les principales forces importantes et des caractéristiques des atomes. Remarquez que l’énergie de maille augmente dans la période et diminue dans le groupe sur le tableau périodique.
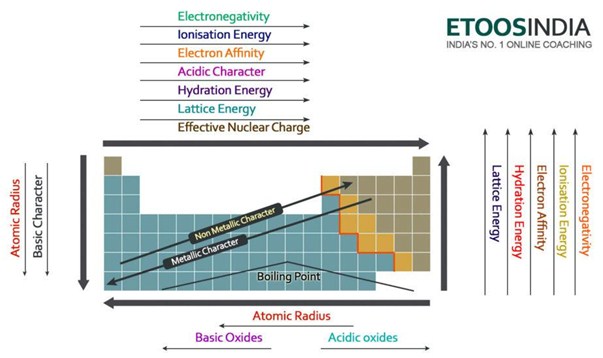
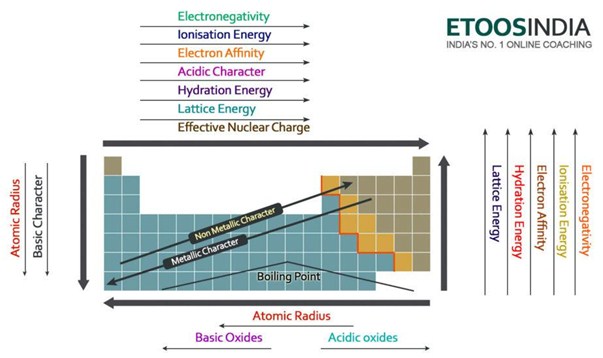
Figure2. Tendances des principales forces et propriétés des atomes dans le tableau périodique. http://blog.etoosindia.com/periodic-table-trends/
Comment calculer les énergies enthalpiques.
Pour calculer l’énergie enthalpique, il faut connaître la loi de Hess :
Le changement d’enthalpie accompagnant un changement chimique est indépendant de la voie par laquelle le changement chimique se produit.
Il faut également définir l’enthalpie d’atomisation, ΔH°a:
L’enthalpie d’atomisation standard est la variation d’enthalpie lorsque 1 mole d’atomes gazeux est formée à partir de l’élément dans son état standard.
La variation d’enthalpie d’atomisation est toujours positive.
Pour calculer les enthalpies, il faut suivre Le cycle de Born-Haber. Il représente une série d’étapes menant à la formation d’un composé ionique à partir des ions gazeux qui le constituent.Le cycle de Born-Haber ne traite que des composés ioniques où les métaux ont tendance à former des cations, et les non-métaux des anions.
Continuons à utiliser NaCl comme exemple pour expliquer le fonctionnement du cycle de Born-Haber.
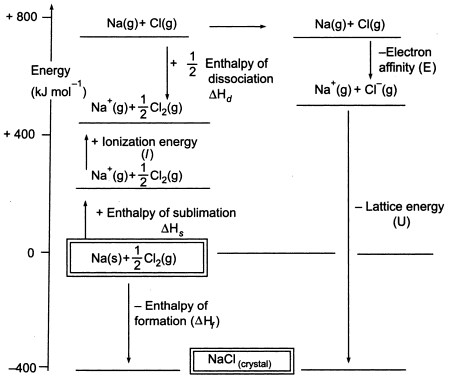
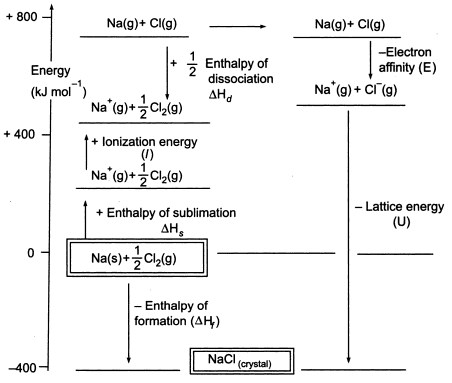
Fig3. Cycle de Born-Haber du NaCl
Comme nous devons produire des atomes gazeux afin de pouvoir utiliser l’étape suivante du cycle, la première étape du cycle implique la formation de sodium métal gazeux à partir de sodium métal solide. Dans cette étape endothermique, l’énergie de sublimation du sodium est de +108 KJ.
La deuxième étape,est également endothermique, et c’est la formation d’un atome de chlore à partir d’une molécule de chlore diatomique car nous devons produire des atomes gazeux afin de pouvoir utiliser l’étape suivante du cycle. L’énergie de dissociation de la liaison de la molécule de chlore diatomique est de +122 KJ.
La troisième étape est l’ionisation de l’atome de sodium gazeux pour former un ion sodium. Comme vous pouvez vous y attendre, le changement d’énergie dans le processus est appelé l’énergie d’ionisation du sodium.Cette étape est endothermique, l’énergie d’ionisation du sodium étant de +496 KJ. Les énergies d’ionisation passent des atomes gazeux aux ions positifs gazeux à charge simple.
La quatrième étape est l’ajout d’un électron à un atome de chlore gazeux, qui est défini comme l’affinité électronique du chlore. Cette étape est exothermique, -349 KJ. Ainsi, à partir des troisième et quatrième étapes, nous obtenons des ions sodium et chlorure. Les affinités électroniques passent des atomes gazeux aux ions négatifs gazeux à charge simple.
Maintenant, la dernière étape consiste à former un cristal de chlorure de sodium à partir des ions sodium et chlorure. Les ions gazeux positifs et négatifs que nous pouvons convertir en chlorure de sodium solide en utilisant l’enthalpie de formation du réseau. Il s’agit de l’énergie de réseau (U), dont la valeur vous sera fournie pour calculer l’enthalpie de réseau ou H. Ici, U du NaCl est de -788 KJ.
Calculons maintenant l’enthalpie de réseau.
Hf = Hsublimation(Na) + Énergie d’ionisation (Na) + Hdissociation(Cl2) + Affinité électronique(Cl) + U (enthalpie de réseau)
.